대장암
이론과 하이라이트 히스토리를 확인 할 수 있어요.
: Colorectal cancer, CRC
거의 매년 국시에 출제된다. 특징적인 임상양상이 주어졌을 때 대장암을 의심하고 대장내시경을 진단한다고 답할 수 있어야 한다. 절제 불가능한 대장암의 고식적 치료에 대한 내용이나 수술 후 추적관찰에 대한 내용도 가끔 출제되며, 가족성 대장암에 대한 내용도 출제된 바 있다. 또한, 국시에서는 종양의 위치나 stage 별로 어떤 술식을 진행하는지도 알고 있어야 하나, 이는 외과의 해당 단원에서 공부하도록 한다. 마지막으로, 대장암은 아니지만 대장의 양성 종양 중 출제된 바 있는 융모샘종에 대해서도 알아야 한다.
1. 개요
1) 역학: 여성보다는 남성에서 약간 더 흔히 발생, 점점 호발 연령이 낮아짐
2) 위험요인: 기저질환(IBD 등), 유전적 소인, 동물성 지방, 비만, 흡연 등
3) 전이: 혈액, 림프절 등을 통해 전이 (간 먼저 → 폐, 뼈, 복막 등)
• 주로 direct extension / 수술 등으로 iatrogenic하게 전이되기도 함
2. 대장 용종(polyp)
1) 병리학적 분류
(1) Non-neoplastic mucosal polyp: Hyperplastic polyp, inflammatory polyp 등
(2) Neoplastic mucosal polyp
① Adenoma: Tubular/tubulovillous/villous로 나뉨 → 추후 악성화 가능
• 이 중 융모샘종(villous adenoma): 분비성 설사 유발 가능
② Carcinoma: Carcinoma in situ, invasive carcinoma
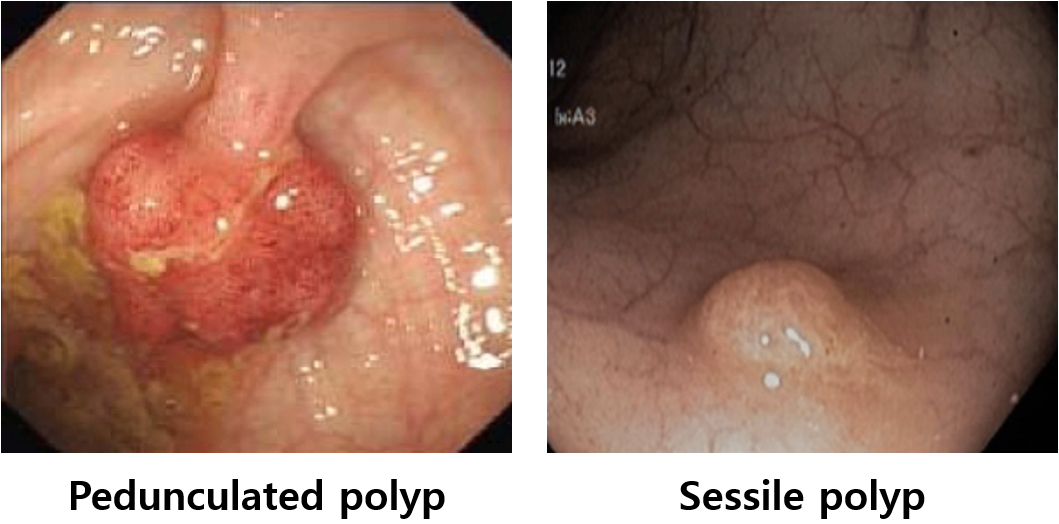
2) 형태학적 분류
(1) 목 있는 폴립(pedunculated polyp): 악성 가능성이 상대적으로 낮음
(2) 목 없는 폴립(sessile polyp): 악성 가능성이 상대적으로 높음
3) 치료
(1) 내시경적 용종절제술(endoscopic polypectomy): 절제 전에는 neoplastic / non-neoplastic 여부를 알 수 없으므로 일단 절제
① 술식
• 내시경점막절제술(endoscopic mucosal resection, EMR)
• 내시경점막하박리술(endoscopic submucosal dissection, ESD)
② 과정: 대장내시경으로 검사하면서 즉석에서 절제 → 조직검사를 시행 후 추가적 치료를 결정
(2) EMR/ESD 후 치료
① 내시경 추적관찰: 아래 3개를 모두 만족할 경우
• 점막하(submucosa) 상위 1/3까지만 침범
* Submucosa 상위 1mm, submucosa 상위 2mm 등 다양한 기준이 존재한다.
• 고분화(grade 1) or 중등도분화(grade 2)
• Lymphovascular invasion 없음
② 대장암에 준하여 추가적 수술: 위 3개 중 하나라도 만족하지 못할 경우
3. 임상양상 및 검사소견
1) 주호소
(1) 혈변: 주로 대변에 섞여 나오는 정도
(2) 변비: 대변이 가늘게 나오거나, 배변 시 복통
(3) 복부덩이: 진행될 경우 외부에서 만져짐
2) 위치에 따른 양상: 대략적인 추세는 아래와 같으며, 항상 일치하는 것은 아님
(1) Cecum, A-colon: 빈혈, 대변 잠혈, 피로
(2) T-colon, D-colon: 변비, 복통
(3) S-colon, rectum: 혈변, 잔변감, 가는 변
* Proximal colon에서는 대변이 상대적으로 액체에 가까우므로 증상이 늦게 나타나며 주로 출혈과 연관되어 있지만, distal colon에서는 대변이 더 단단해지므로 obstruction 관련 증상들이 나타나기 시작한다.
3) 종양 표지자: CEA 상승 (상승했다고 해서 항상 대장암인 것은 아님)
4. 진단
1) 대장암 여부 확인
(1) 직장수지검사(digital rectal examination, DRE)
① 만져지는 종괴가 있는지(직장암일 경우), 혈변이 묻어나오는지 확인
② 직장 선반(rectal shelf)이 만져질 경우 암종의 복막전이를 의심
* Rectal shelf = Rectovesical / rectouterine pouch에 peritoneum의 전이성 종양이 만져지는 것
(2) 대변잠혈검사: 주로 선별검사 목적으로 사용됨
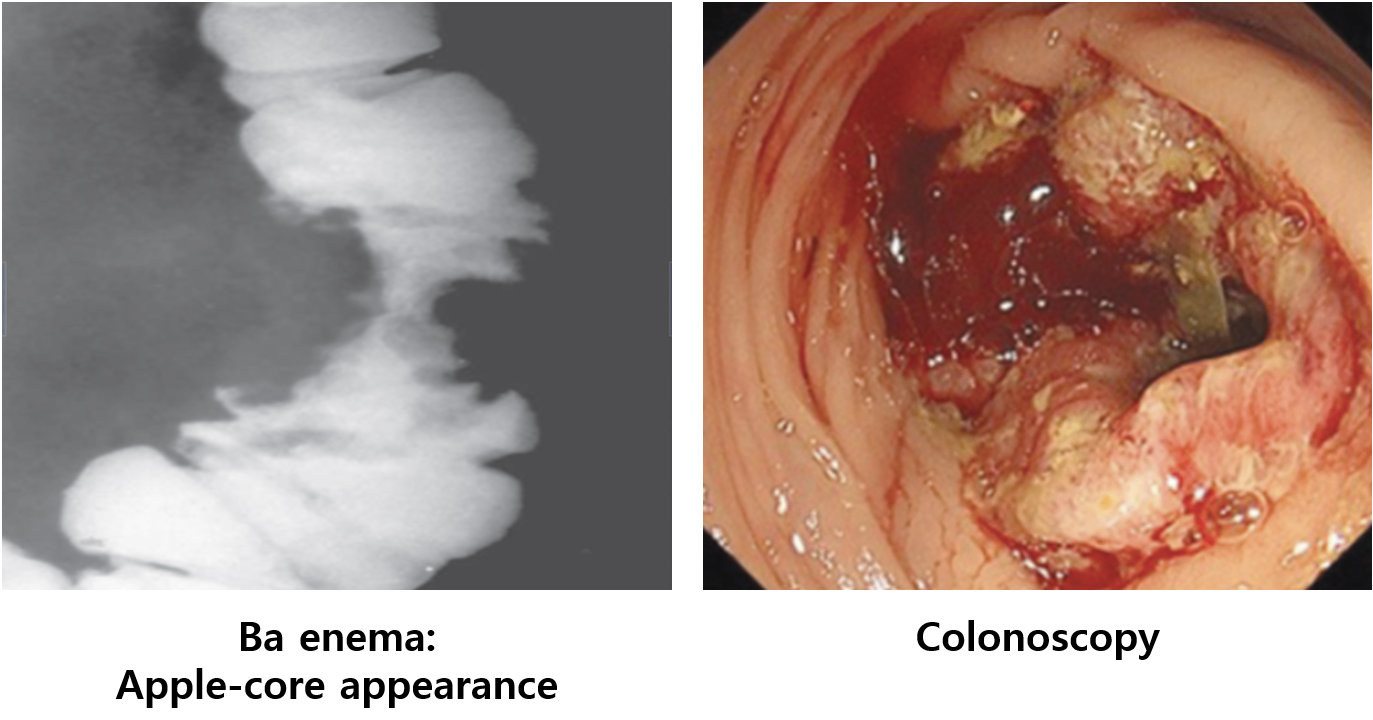
(3) Barium enema: 내강이 좁아진 구조 관찰(apple-core appearance)
(4) 대장내시경: 확진 위해 시행 → 병변 확인 → 조직검사
(5) 경피적 조직검사: 복막 전이에서 조직생검이 용이할 경우 대장내시경을 통하지 않고 시행
2) 병기 설정(staging)
(1) 복부 CT, MRI, PET
(2) 내시경초음파(endoscopic ultrasound, EUS): 침윤 깊이 확인
* 자세한 내용은 ‘대장암의 병기’ 참고
5. 치료
1) Stage I~III: 대장암의 외과적 접근’ 참고
(1) 결장암(colon cancer): 수술 (+ stage에 따라 adjuvant CTx)
(2) 직장암(rectal cancer): 수술 (+ stage에 따라 neoadj. CCRT)
(3) 수술(+ CTx/CCRT) 후: CEA로 추적관찰
• 치료 후 CEA가 다시 증가하는 경우, 재발을 의심해야 함
2) Stage IV 전이성 대장암
(1) 항암화학요법: 주로 5-fluorouracil, capecitabine, irinotecan, oxaliplatin 등이 사용됨
(2) 간/폐 전이 단일 병변의 경우 수술적 절제 고려할 수 있음
3) 장폐색에 대한 치료
(1) 내시경적 감압술
(2) 대장 스텐트 삽입
(3) 고식적(palliative) 수술: Negative margin을 고려해 크게 절제하지 않고, 장폐색을 호전시킬 수 있을 정도만 절제
• 주로 완전폐색이나, 폐색으로 인해 ischemia 등이 발생했을 때 고려
6. 가족성 대장암
1) 가족성 선종성 용종증(familial adenomatous polyposis, FAP)
(1) 병태생리
① 주로 autosomal dominant 형태로 유전 (단, 가족력 없이 sporadic mutation으로도 발병 가능)
② 5번 염색체의 long arm의 deletion → APC gene mutation → tumor suppressor gene의 소실
③ 전 대장에 걸쳐 수천 개의 polyp이 생성 → 거의 모든 환자가 40세 이전에 대장암 발병
(2) 검사소견: 하부위장관 내시경 - 대장 전체에 골고루 매우 많은 수의 polyp
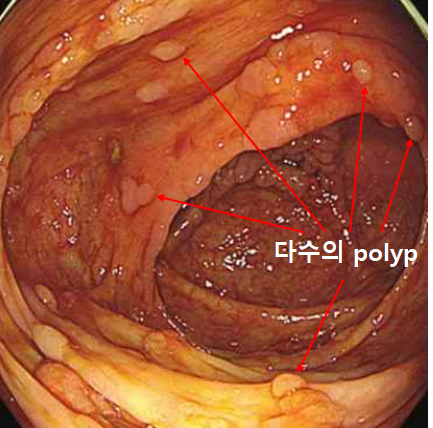
(3) 치료/예방: 전결장절제술(total colectomy) + 추적 관찰
2) 유전성 비용종성 대장암(hereditary non-polyposis colon cancer, HNPCC, Lynch syndrome)
(1) 병태생리
① hMSH2, hMLH1 등의 mismatch repair gene의 선천적인 손상
② Microsatellite instability(MSI) 발생 → DNA 복제시 유전적 결함 발생률의 증가
③ TGFβRⅡ, BAX 등 변이에 취약한 유전자들에서 변이 발생
난소/자궁/위 등의 암
(2) 임상양상
① Proximal colon(ascending 등)에 주로 발생
② 난소/자궁/위 등의 암과 연관되어 있음
(3) 추적관찰: 30~40대에 주로 발병하므로, 25세부터 1~2년마다 colonoscopy 시행
대장암 정리 | |
임상양상 | • 변비, 혈변, 복부덩이, 체중감소 등 |
진단 | • DRE(직장선반 촉진시 전이성 직장암) → 대장내시경 • 병기 설정: CT, MRI, PET, EUS 등 |
치료 | • 대장 용종: EMR/ESD → submucosa 1/3 이상 침범시 수술 • Stage I(≤ 근육층): 수술 • Stage II~III(원격전이 없음) - 결장암: 수술 (+ adj. CTx) / 직장암: Neoadj. CCRT + 수술 • Stage IV(원격전이): 항암치료 - 간/폐 단일 병변시 수술적 절제 가능 - 장폐색시 stent 삽입, 고식적 수술 |
Harrison 21e, pp.636-643
NCCN guideline, 2024-5(colon)
NCCN guideline, 2024-4(rectal)