대사성 산증
이론과 하이라이트 히스토리를 확인 할 수 있어요.
: Metabolic acidosis, MAc
국시에는 주로 만성신부전, 패혈증, 당뇨병성 케톤산증 등과 연관되어 출제되는데, 대부분 대사성 산증이 있음을 인지하기만 하면 되는 문제들이다. 하지만 대사성 산증의 진단적 접근에 대해서도 드물지만 출제되기는 하며, 이해하고 있다면 쉽지만 모른다면 찍기조차 어려울 가능성이 높으므로 내용을 숙지하는 것을 권한다. 크게 serum anion gap을 계산하고, 결과값에 따라 high anion gap, normal anion gap 질환들로 나뉜다는 개념과 그 의미를 잡고 있으면 크게 어렵지 않을 것이다. 신세뇨관 산증(RTA)은 다른 단원에서 자세히 다루고 있다.
1. 원인
1) H+ 증가
(1) 체내 H+ 생성
① Lactic acidosis: Shock 상태 → tissue perfusion↓ → anaerobic metabolism → 젖산 생성↑
② Ketoacidosis: 지방산 대사량↑ → acetoacetate, β-hydroxybutyrate 등 생성
• Diabetic ketoacidosis(DKA): Insulin 결핍으로 인한 지방산 유리 및 대사 증가
• Alcoholic ketoacidosis(AKA): 장기간 음주로 인한 glucose 결핍으로 인한 지방산 유리 및 대사 증가
• Starvation ketoacidosis: 장기간 금식/영양실조로 인한 glucose 결핍으로 인한 지방산 유리 및 대사 증가
(2) 체외 H+ 유입
• Ethylene glycol, methanol, propylene glycol, salicylate 등: 응급의학과 독성학 참고
2) HCO3- 소실
(1) Extrarenal
• 설사, 담즙/췌장액 소실: 소장액은 알칼리성이므로 대량 배출시 HCO3- 소실이 증가
(2) Renal
① HCO3-의 직접적 소실: 신세뇨관 산증 type II
② H+의 배설 감소: AKI, CKD, 신세뇨관 산증 type I/IV
• Collecting duct에서 H+가 배설되지 않음 → H2CO3에서 H+와 HCO3-를 생성하는 반응이 일어나지 않음 → HCO3- 흡수량↓
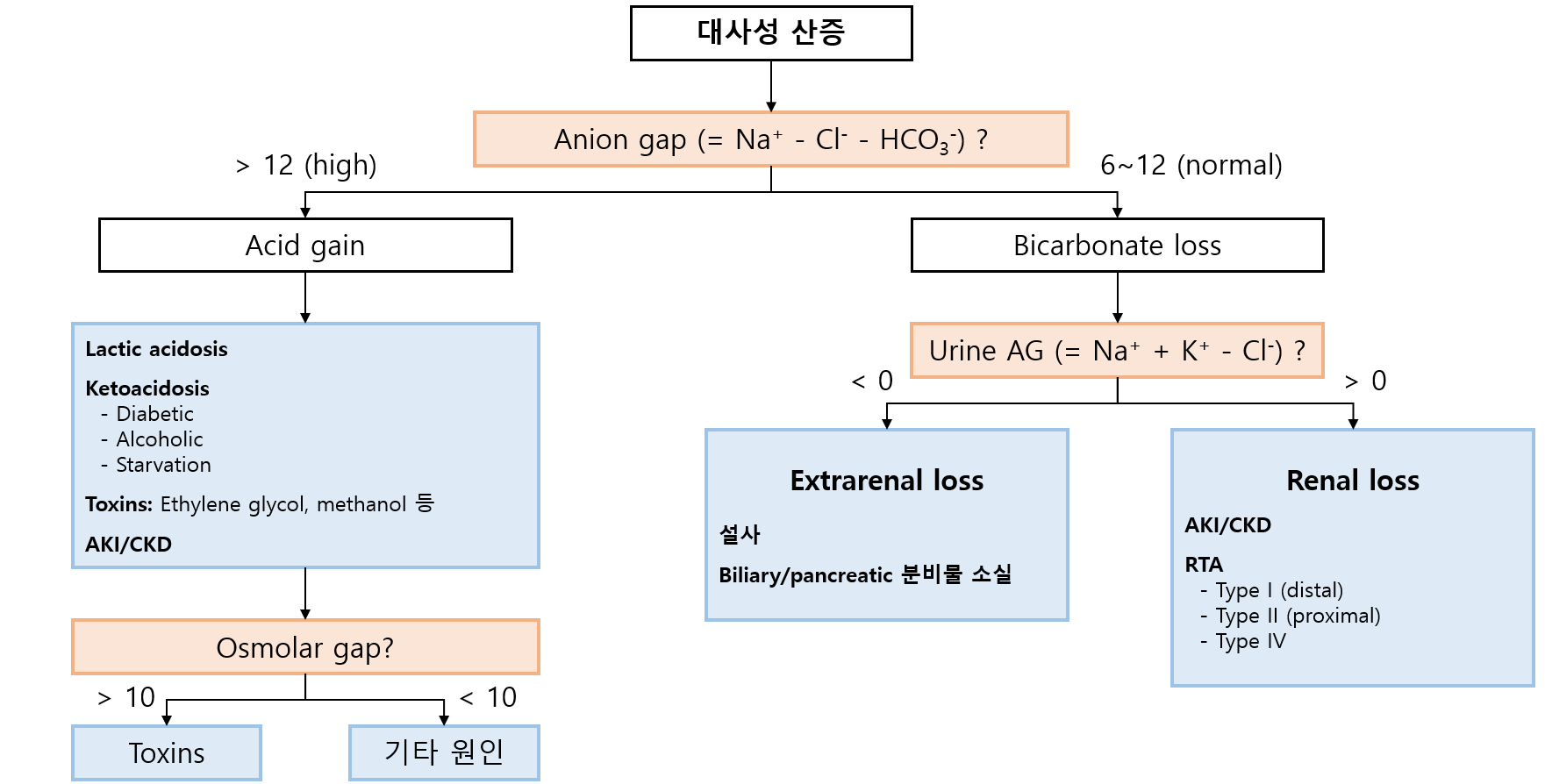
* 대체로 위의 'H+ 증가'는 하술할 high AG에, 'HCO3- 소실'은 normal AG에 해당한다. 'H+의 증가' 중 '체내 H+ 생성'은 normal osmolar gap을, '체외 H+ 유입'은 high osmolar gap을 시사한다. 'HCO3- 소실' 중 'extrarenal'은 urine AG < 0을, 'renal'은 urine AG > 0을 시사한다. 아래 진단적 접근의 각 단계를 각 대사성 산증의 원인과 연결지어 공부하면 더 수월하게 이해할 수 있다.
2. 초기 진단적 접근
1) 대사성 산증의 진단
(1) pH < 7.35
(2) HCO3- 감소
(3) PaCO2 감소: 호흡성 보상의 적절성은 아래 중 하나로 판단
① HCO3- 1 감소 → PaCO2 1.2~1.25 감소
② PaCO2 = 1.5×[HCO3-] + 8 ± 2
③ PaCO2 = [HCO3-] + 15
2) 음이온 차(anion gap, AG) 계산
(1) 정의: AG = Na+ - (Cl- + HCO3-)
(2) 의미
① 혈중 양이온과 음이온은 전기적 평형을 이루고 있음
• 양이온: Na+ (K+, Ca2+, Mg2+ 등은 무시함)
• 음이온: Cl-, HCO3-, 기타 음이온(protein, phosphate, lactate, organic acids)
② 전기적 평형을 가정하면 Na+ = Cl- + HCO3- + 기타 음이온
③ ∴ AG = [기타 음이온]
(3) 해석
① High AG: > 12 mEq/L - H+ 증가
• 혈액 내 새로운 산이 증가 (HA → H+ + A-)
• H+가 HCO3-를 소모시킴 (H+ + HCO3- → H2O + CO2)
• 남은 A-는 그대로 쌓이고, HCO3-는 감소했으므로 AG↑
② Normal AG: 6~12 mEq/L - HCO3- 소실
• 새로운 A-의 유입 없이 HCO3-만 감소함
• 음이온인 HCO3-의 빈자리를 음이온인 Cl- → AG 변화없음
* 이 때문에 normal AG metabolic acidosis를 hyperchloremic MAc라고도 한다. 문헌에 따라 non-AG MAc라고도 부른다.
* AG의 어디까지가 normal이고 어디부터가 high인지에 대해서 명확히 정립된 바는 없다. 알렌의 서재는 12 mEq/L을 기준으로 삼고 있으며, 이는 Harrison 21e, UpToDate 등의 다양한 문헌을 종합적으로 고려하여 국시에 가장 적절하다고 판단되는 수치다.
* AG < 4 mEq/L일 경우 low AG라고도 부르지만, 이는 극히 드물다. AG 계산에서 무시했던 양이온이 많을 때 주로 발생한다. ex) severe hyperK/hyperCa, IgG 증가 등
* AG는 albumin에 영향을 받으므로, hypoalbuminemia가 있다면 이에 따른 보정을 해주어야 한다. Albumin이 정상(4.5 g/dL)에서 1 g/dL 감소할 때마다 AG에 2.5 mEq/L을 더해주어야 한다.
3. High AG 대사성 산증
1) 진단: 대부분 병력청취, 기본적인 혈액/소변검사만으로도 추정진단을 잡을 수 있음
H+ 증가 | 체내 H+ 생성 | • Lactic acidosis, ketoacidosis(diabetic, alcoholic, starvation) 등 |
체외 H+ 유입 | • Ethylene glycol, methanol, propylene glycol, salicylates 등 | |
HCO3- 소실* | • AKI, CKD | |
(1) Lactate↑: Lactic acidosis
(2) Urine ketone(+), glucose(+): Diabetic ketoacidosis
(3) Urine ketone(+), glucose(-): Alcoholic/starvation ketoacidosis → 음주 병력으로 둘을 구분
(4) BUN/Cr↑: AKI/CKD
* AKI/CKD가 MAc를 일으키는 이유는 정상적인 네프론의 수가 부족해짐에 따라 H+를 제대로 배설하지 못하기 때문이다. 이는 보통 normal AG MAc를 일으키나, AKI/CKD의 GFR이 매우 낮아지면(< 15~20 mL/min) 소변으로 배출되어야 하는 음이온(phosphate, lactate 등)을 배출하는 기능마저 낮아지게 된다. 이는 AG 계산에 있어 '기타 음이온'으로 잡히기 때문에, high AG MAc의 형태로 나타나게 된다.
2) 오스몰 차(osmolar gap, OG): 원인이 명확하지 않을 때
(1) 정의: OG = 측정한 osmolality - 계산한 osmolality
① 측정한 osmolality: 2×[Na+] + [glucose]/18 + [BUN]/2.8 + unmeasured osmolality (혈액검사 기계가 측정한 수치)
② 계산한 osmolality: 2×[Na+] + [glucose]/18 + [BUN]/2.8 (의사가 각 수치를 대입해 직접 계산)
③ ∴ OG = Unmeasured osmolality
(2) 해석: OG > 10 → osmolality를 증가시키는 미상의 물질이 외부에서 들어왔음을 시사함
ex) Ethylene glycol, methanol, propylene glycol, salicylates 등
3) 치료
(1) 원인 질환 치료
(2) Bicarbonate therapy
① Lactic acidosis, ketoacidosis: 매우 심한 산증(pH < 7.0~7.1) or 중증 신기능 장애 동반시에만 고려
* Lactate, ketoacid 등은 acidosis가 해소되면 추후 HCO3-로 대사될 수 있으므로 HCO3-의 투여는 오히려 해로울 수 있다. 단, 산증이 너무 심할 경우 심기능 저하 등이 발생할 수 있으므로 조심스럽게 HCO3-를 투여해볼 수 있다.
② 물질 중독, AKI/CKD: 위 질환보다는 적극적으로 고려
4. Normal AG 대사성 산증
1) 진단: 설사 병력, BUN/Cr 검사 등으로 대략적인 추정진단은 잡을 수 있음
HCO3- 소실 | Extrarenal | • 설사, 담즙/췌장액 소실 |
Renal | • HCO3-의 직접적 소실: 신세뇨관 산증 type II • H+의 배설 감소: AKI, CKD, 신세뇨관 산증 type I/IV |
2) 요 음이온 차(urine anion gap, urine AG): Extrarenal과 renal 원인을 구분
(1) 정의: Urine AG = Na+ + K+ - Cl-
(2) 의미
① 소변 양이온과 음이온은 전기적 평형을 이루고 있음
• 양이온: Na+, K+, 기타 양이온(대부분 NH4+)
• 음이온: Cl- (기타 음이온은 무시됨)
② 전기적 평형을 가정하면 Na+ + K+ + NH4+ = Cl-
③ ∴ Urine AG = - [NH4+] = 신장의 H+ 배설을 반영하는 지표
* 신장은 H+를 배설하기 위해 NH3를 합성해 NH4+로 결합시켜 배출하기 때문이다.

(3) 해석
① Urine AG < 0: Extrarenal loss
• Urine AG = -[NH4+] < 0 ⇔ [NH4+] > 0
• 신장 외 기관에서 HCO3-이 소실되고 있으므로 신장은 H+를 NH4+의 형태로 배출하려고 하는 중
② Urine AG > 0: Renal loss
• Urine AG = -[NH4+] > 0 ⇔ [NH4+] < 0
• 신장이 H+를 배출하지 못하므로 NH4+도 배출되지 않음
3) 치료
(1) 원인 질환 치료
(2) Bicarbonate therapy: HCO3-가 소실되고 있으므로 이를 보충해줌
(3) 필요시 K+ 보충: Acidosis 교정시 K+가 세포 밖 → 세포 안으로 이동해 hypoK 가능하므로 이에 대해 예방적으로 투여 고려
5. 혼합성 대사성 산-염기 장애
1) ΔAG / ΔHCO3-: 혼합성 대사성 산-염기 장애를 진단할 때 사용되는 지표
(1) ΔAG = | 환자의 AG - 정상 AG(10) |
(2) ΔHCO3- = | 정상 HCO3-(24) - 환자의 HCO3- |
2) 의미
(1) 일반적인 high AG MAc에서 산(HA → H+ + A-)의 H+는 HCO3-와 1:1로 반응함
(2) 따라서 A-의 생성량(= ΔAG)과 HCO3-의 소실량(= ΔHCO3-)은 1:1로 같아야 함
(3) 그러나 기타 산-염기 장애가 동반되어 있을 경우 ΔAG와 ΔHCO3-의 비율이 달라질 수 있음
3) 해석
(1) ΔAG/ΔHCO3- < 1: High AG MAc 외에 HCO3-를 감소시키는 다른 문제가 존재함
ex) High AG MAc + normal AG MAc: pH 7.20, PaCO2 25, HCO3- 10, Na+/K+/Cl- 135/3.0/110일 때, MAc에 대한 호흡성 보상은 제대로 이루어지고 있다. AG = 135-110-10 = 15 > 12이므로 high AG MAc이다. 그런데 ΔAG는 15-10 = 5, ΔHCO3- = 24-10 = 14로 큰 차이가 난다. 이는 HCO3-를 감소시키는 추가적 원인이 있음을 의미하며, 현재 호흡성 보상은 적절하므로 가능한 원인은 normal AG MAc밖에 없다. 예를 들어, 심한 설사로 인해 normal AG MAc가 있는데, 설사로 인한 hypovolemic shock에 의해 lactic acidosis가 발생할 경우 위와 같은 수치들이 나타날 수 있다.
(2) ΔAG/ΔHCO3- > 2: High AG MAc에 반하여 HCO3-를 증가시키는 다른 문제가 존재함
ex) High AG MAc + metabolic alkalosis: pH 7.42, PaCO2 40, HCO3- 25, Na+/K+/Cl- 140/3.0/95일 때, 언뜻 보면 산-염기 장애가 없는 것처럼 보인다. 하지만 AG를 계산해보면 140-95-25 = 20 > 12이므로 high AG 상태이다. ΔAG는 20-10 = 10, ΔHCO3- = |24-25| = 1로 큰 차이가 난다. 이는 high AG MAc가 있지만, HCO3-를 증가시켜 산-염기 상태가 정상적인 것처럼 착각시키는 원인, 즉 metabolic alkalosis(MAlk)가 있음을 의미한다. 예를 들어, CKD가 심해 high AG MAc가 있는 환자에게 요독증으로 인한 구토가 지속되어 MAlk가 동반될 경우 위와 같은 수치들이 나타날 수 있다. 추후 바이탈 과 수련 계획이 있다면, ABGA 결과가 정상인 것 같더라도 AG를 계산해보는 습관을 들여야 한다.
Harrison 22e, pp.369-373