신장 생리
이론과 하이라이트 히스토리를 확인 할 수 있어요.
시험에 직접적으로 출제되는 부분은 아니지만 신장 과목을 공부하는데 가장 기본이 되는 내용이다. 이 내용을 잘 이해해야 신장 질환에서 발생하는 각종 혈량 불균형, 전해질 불균형, 산-염기 불균형, 이뇨제의 효과 및 부작용을 제대로 이해할 수 있다. 신장의 복잡한 생리를 이해할 자신이 없다면 각 질환에서 나타나는 각종 이상소견을 무작정 외우는 것도 불가능한 방법은 아니지만, 휘발성이 매우 강할 것이므로 본 단원의 내용을 머릿속에 새겨두는 것을 권한다.
1. 수분 및 전해질 대사 총론
1) Body fluid compartment
• Total body fluid: 남자는 체중의 60%, 여자는 체중의 50%
TBF (total body fluid) 60% of body weight | ICF (intracellular fluid, 세포내액) 40% (2/3) | |
ECF (extracellular fluid, 세포외액) 20% (1/3) | ISF (interstitial fluid, 세포간질액) 15% (3/4) | |
Plasma (혈장) 5% (1/4) | ||
2) Serum osmolality (혈장 오스몰)
(1) 정의: 물 1kg에 포함된 solute 농도. Membrane을 통한 water shift에 영향을 주기 때문에 중요
(2) 정상범위: 275~295 mOsm/kgH2O
(3) Calculated osmolality: 2×[Na+] + [Glucose]/18 + [BUN]/2.8
① [Na+] ≒ (총 cation 양) = (총 anion 양) 이므로, (총 ion 양 ) ≒ 2×[Na+]
② Glucose의 분자량 = 180g/mol, 따라서 mg/dL을 mmol/L로 환산 → [Glucose]/18
③ Urea의 질소 분자량 = 14×2 = 28g/mol, 따라서 mg/dL을 mmol/L로 환산 → [BUN]/2.8
* Serum osmolality에 영향을 미치는 주요 물질은 ion, glucose, urea이다. Na+, glucose, BUN 농도만으로 실제 osmolality를 이론적으로 예측한 값이 calculated osmolality다.
(4) Effective osmoles: Na+, glucose 등
① ICF 또는 ECF 중 어느 한 곳에만 머물고 이동하지 않음
② 삼투압 형성, cell membrane을 통한 water shift에 영향
(5) Ineffective osmoles: Urea 등
① ICF와 ECF 사이에서 자유롭게 확산
② 삼투압 형성 안함, cell membrane을 통한 water shift에 영향 없음
(6) 따라서 effective osmolality = 2×[Na+] + [Glucose]/18
2. 신장의 기능
1) 배설 기능
(1) 대사 부산물: Urea, creatinine, ammonia, uric acid, organic/inorganic acids
(2) 외부 물질: Drug, toxin 등
2) 조절 기능: 소변을 내보내는 과정에서 여러 성분들을 재흡수/배설해서 몸의 항상성 유지
(1) 체액의 volume과 osmolality
(2) 전해질 균형
(3) 산-염기 평형
3) 내분비 기능
(1) Renin: 간에서 생성된 angiotensinogen을 angiotensin I으로 전환
(2) Prostaglandin(PGE2 등): Afferent arteriole vasodilation, collecting duct에서 ADH를 분해해서 더 이상 작용하지 못하도록 함
(3) Erythropoietin(EPO): 적혈구 생성 촉진
(4) Vit. D(1,25-dihydroxyvitamin D3): 체내 Ca, phosphate 평형에 중요
4) 대사 기능: Gluconeogenesis
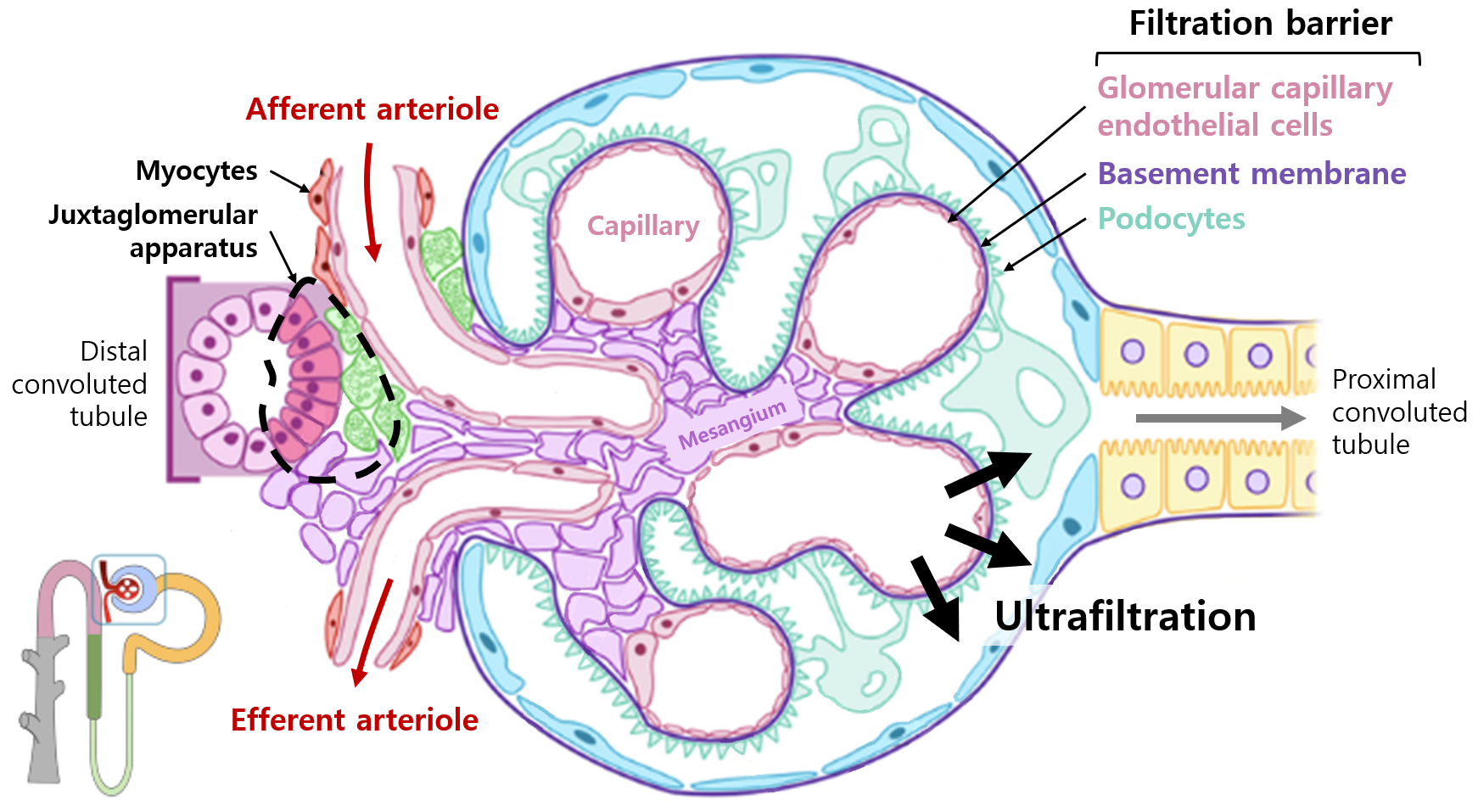
3. 사구체(glomerulus, 콩팥토리)
1) 기능: Ultrafiltration
(1) 혈관 → 세뇨관으로 수분, 전해질, 노폐물을 일괄적으로 여과시킴
(2) Filtration barrier가 '무엇을 여과시킬지'를 결정
(3) Myocytes, juxtaglomerular apparatus가 '얼마나 여과시킬지'를 결정
2) Filtration barrier
(1) 구조
① 사구체 모세혈관 내피세포(glomerular capillary endothelial cells)
• 내피세포 사이사이에 구멍이 뚫린 것처럼 빈 공간이 존재함(fenestration) → 이 틈으로 물질들이 여과됨
② 사구체 기저막(glomerular basement membrane, GBM)
• 음전하를 나타내는 막
③ 족세포(podocyte)
• 족세포의 foot process가 깍지 끼듯이 사구체를 감싸고 있음 (깍지 사이의 작은 공간 = slit diaphragm)
(2) 위 ①~③이 얽혀 음전하를 띠며 4 nm 크기의 구멍들이 뚫린 filtration barrier를 형성
* 이 때문에 음전하를 띠는 albumin은 크기가 4 nm보다 약간 작아도 거의 정상적인 filtration barrier를 통과하지 못한다.
3) 사구체여과율(glomerular filtration rate, GFR)의 조절
(1) Afferent arteriole myocyte
① Renal a. 압력↑ → aff. arteriole 수축 → GFR↓
② Renal a. 압력↓ → aff. arteriole 이완 → GFR↑
(2) Tubuloglomerular feedback(TGF)
① Juxtaglomerular apparatus의 일부인 macula densa(distal tubule에 위치)가 distal tubule에 도달한 solute 양을 감지함
② GFR↑ → 많은 양의 solute가 DT로 흘러들어감 → MD가 이를 감지 → aff. arteriole 수축 → GFR↓
③ GFR↓ → 적은 양의 solute가 DT로 흘러들어감 → MD가 이를 감지 → aff. arteriole 이완 → GFR↑
(3) Angiotensin-II
① Juxtaglomerular apparatus의 일부인 granular cell(aff. arteriole에 위치)가 arteriole로 들어오는 혈류를 감지함
② GFR↑ → GC가 이를 감지 → renin 분비↓ → RAAS 억제 → angiotensin-II↓ → eff. arteriole 이완 → GFR↓
③ GFR↓ → GC가 이를 감지 → renin 분비↑ → RAAS 활성 → angiotensin-II↑ → eff. arteriole 수축 → GFR↑
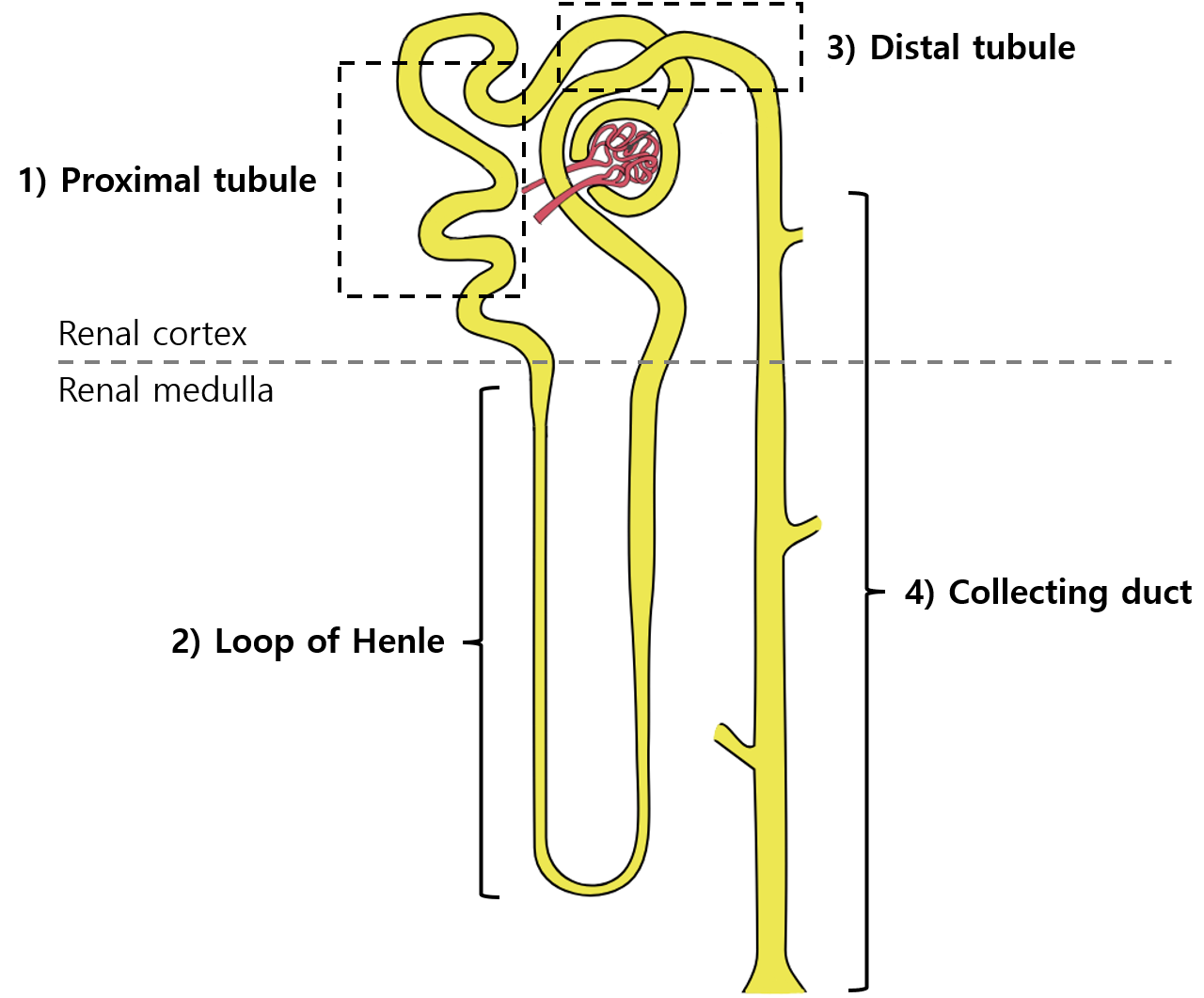
4. 세뇨관(tubule)
* 후술할 세뇨관에서 이루어지는 거의 모든 재흡수/분비 과정은 tubule 세포의 interstitium 쪽에 있는 Na+/K+ ATPase pump가 생성하는 Na+ gradient를 에너지 기반으로 하여 이루어진다. Na+를 세포 내부에서 interstitium 쪽으로 퍼내면 세포 내부의 Na+는 상대적으로 부족해지게 되고, 이에 따라 tubular lumen에서 세포 내부로 Na+가 이동하는 것이다. 이 Na+의 이동을 따라 다른 물질들이 같이 유입되기도 하고(cotransport), 반대 방향으로 배출되기도 한다(exchange).
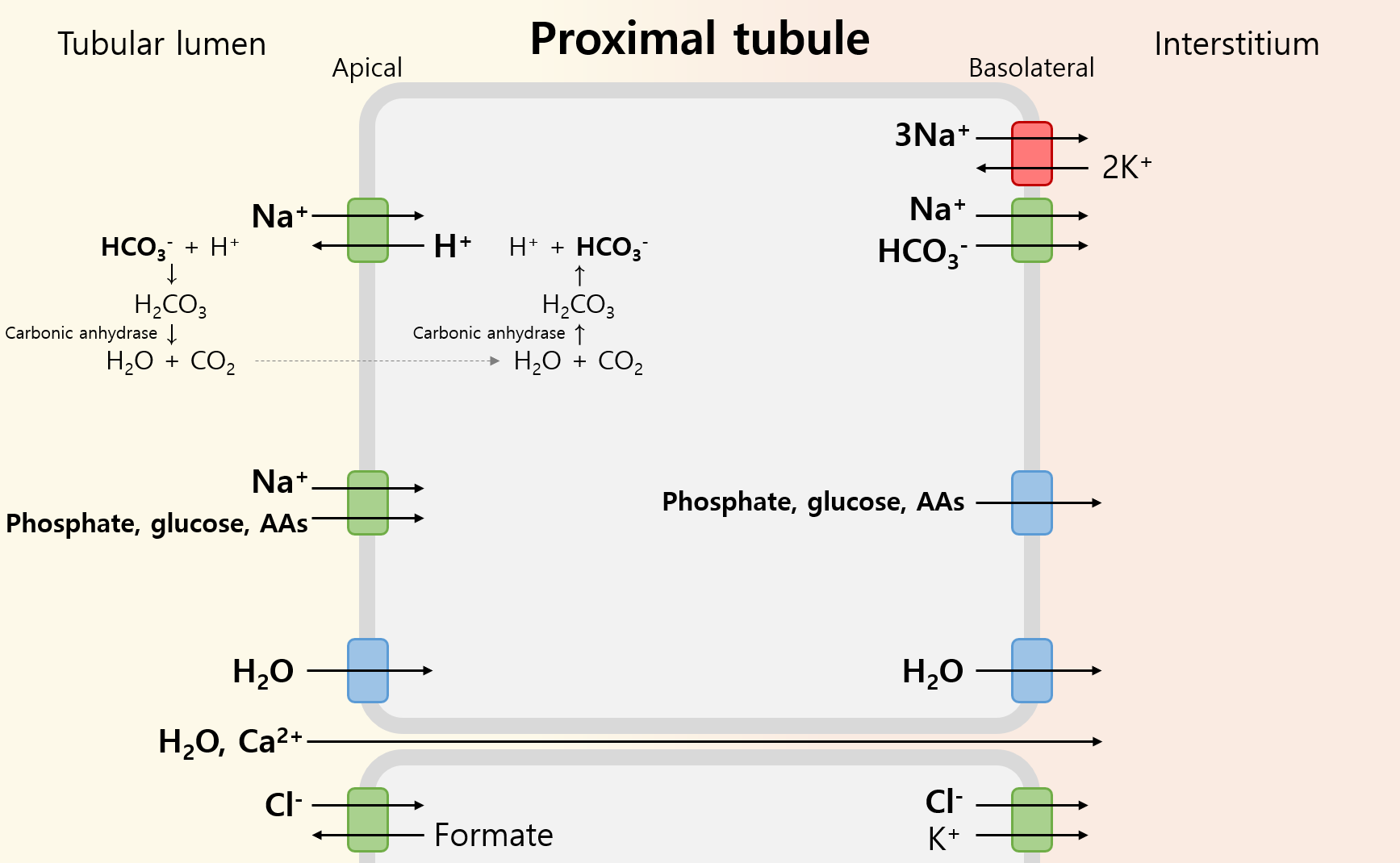
1) 근위 세뇨관(proximal tubule, PT)
(1) 기능: 사구체에서 여과된 물질의 약 70%를 재흡수(bulk reabsorption)
① 재흡수: H2O, Na+, Cl-, HCO3-, Ca2+, phosphate, glucose, amino acids 등
② 분비: H+, 기타 organic acids/bases
(2) 관련 주요 물질
H2O | 세포 사이로(paracellular) 확산 또는 aquaporin channel을 통한 수송 |
Na+ | ① Basolateral에서 Na+/K+ pump에 의해 세포 내부의 Na+↓ ② Apical에서 다양한 물질들과 함께 흡수 |
H+ | Na+가 흡수될 때 반대 방향으로 분비됨 (분비된 H+는 NH3 등과 결합해 NH4+ 등의 형태로 배설) |
HCO3- | ① 분비된 H+가 HCO3-와 tubular lumen에서 H2CO3로 결합 ② Carbonic anhydrase(CA)에 의해 H2O + CO2로 분리 ③ CO2는 nonpolar하므로 세포 내부로 확산 ④ H2O와 함께 CA에 의해 다시 H2CO3로 재결합 → H+ + HCO3-로 분리 |
Phosphate | Na+가 흡수될 때 같은 방향으로 흡수됨 * 칼슘/인 대사에서 혈중 Pi가 높을 때 FGF-23가 이 수송체를 억제해 Pi의 신장 재흡수를 억제한다. |
Glucose | Na+가 흡수될 때 같은 방향으로 흡수됨 * 이 수송체의 이름이 SGLT-2로, 당뇨 치료제 SGLT-2 inhibitor는 이를 억제해 glucose의 신장 재흡수를 억제한다. |
(3) 관련 질환: Fanconi syndrome
① Proximal tubule의 모든 cotransporter의 기능 상실
② Acidosis(H+ 분비↓, HCO3- 재흡수↓), hypophosphatemia(Pi 재흡수↓)
(4) 관련 이뇨제: CA inhibitor(acetazolamide)
① 원리: CA 억제 → HCO3- 재흡수↓ → 세포 내 H+ 생성↓ → Na+/H+ exchange↓ → Na+ 재흡수↓ → 이뇨 작용
② 부작용: 신세뇨관 산증(HCO3- 재흡수↓ → 혈중 pH↓)
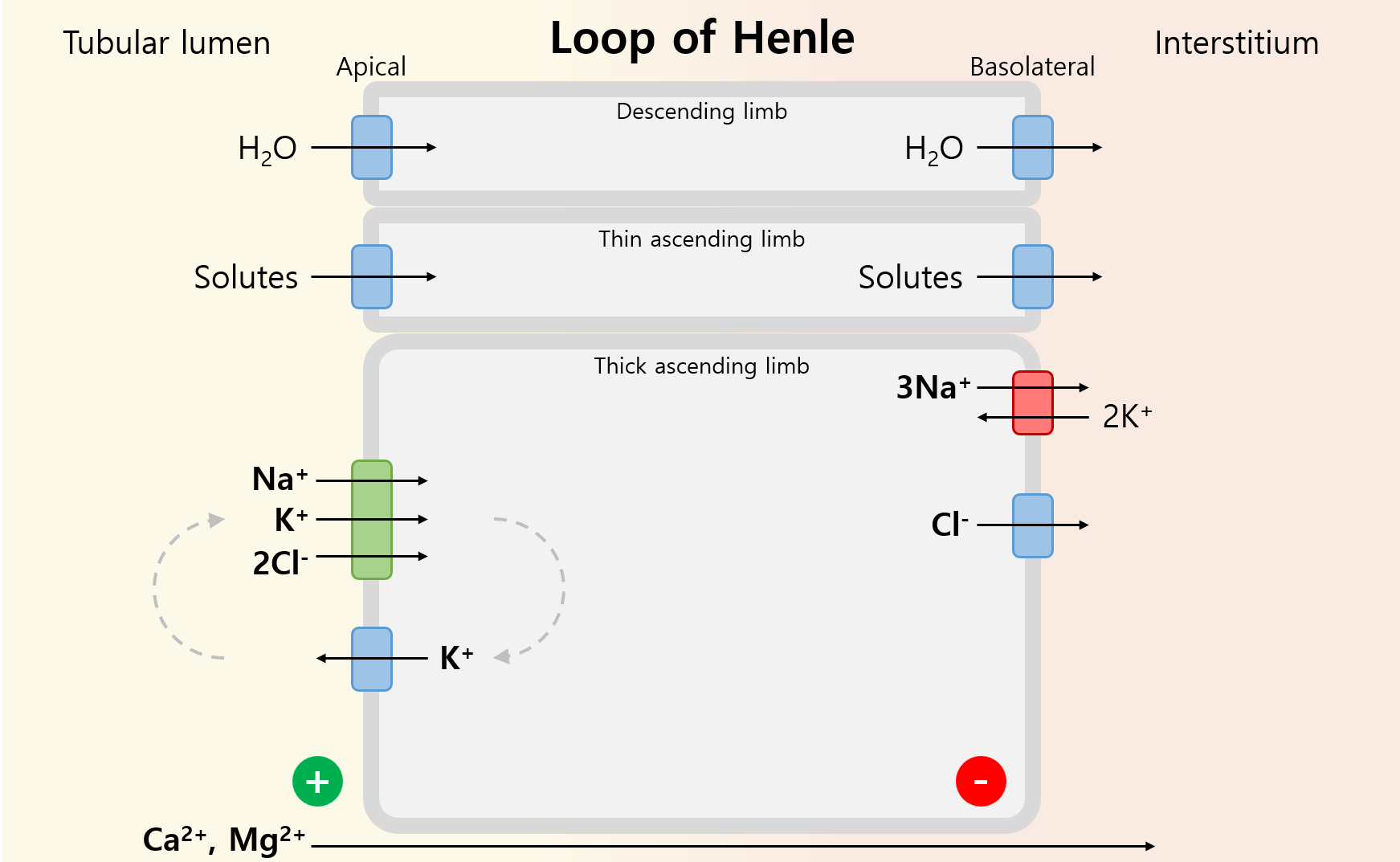
2) 헨레 고리(loop of Henle, LoH)
(1) 기능: Na+/Cl-/Ca2+ 재흡수, 요농축을 위한 countercurrent multiplication
① Descending limb: H2O만 투과 가능, solute 투과 불가능
② Thin ascending limb: Solute만 투과 가능, H2O 투과 불가능
③ Thick ascending limb: NKCC 등 수송체를 이용해 solute 투과 가능, H2O 투과 불가능
(2) 관련 주요 물질
Na+ | ① Basolateral에서 Na+/K+ pump에 의해 세포 내부의 Na+↓ ② Apical에서 Na+/K+/2Cl- channel(NKCC)를 통해 흡수 |
K+ | ① Na+가 흡수될 때 같은 방향으로 NKCC를 통해 흡수 ② K+ channel을 통해 다시 tubular lumen으로 분비 (K+ recycling) |
Cl- | Na+가 흡수될 때 같은 방향으로 NKCC를 통해 흡수 |
Ca2+/Mg2+ | ① Apical에서 K+가 분비되며 tubular lumen은 (+), 다른 곳은 (-) 전하를 띠게 됨 ② Electrical gradient에 따라 양이온인 Ca2+/Mg2+가 paracellular하게 interstitium으로 이동 |
(3) 관련 질환: Bartter's syndrome
① Thick ascending limb에 관여하는 수송체(NKCC 등)의 기능 상실
② 저혈량(Na+ 재흡수↓), hypoK/alkalosis(저혈량에 대한 aldosterone↑ 등), 요로결석(urine Ca2+↑)
(4) 관련 이뇨제: 고리이뇨제(loop diuretics - furosemide, torsemide 등)
① 원리: NKCC 억제 → Na+ 재흡수↓ → 이뇨 작용
② 부작용: HypoCa(NKCC 억제 → K+ 유입↓ → 다시 배출될 K+가 부족함 → electrical gradient 소실 → Ca2+ 이동 불가)
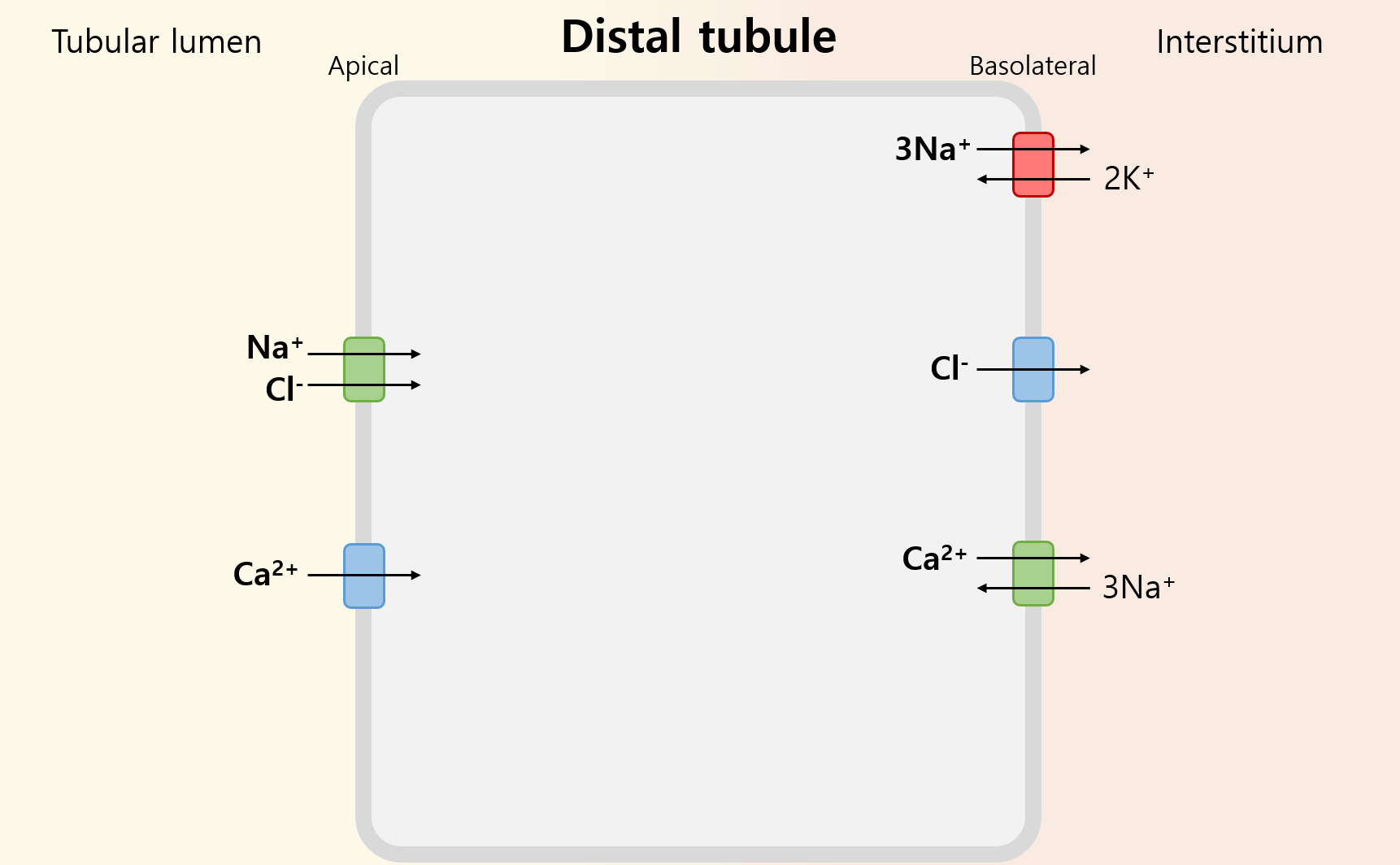
3) 원위 세뇨관(distal tubule, DT)
(1) 기능: Na+/Cl-/Ca2+ 재흡수
(2) 관련 주요 물질
Na+ | ① Basolateral에서 Na+/K+ pump에 의해 세포 내부의 Na+↓ ② Apical에서 Na+/Cl- channel(NCC)를 통해 흡수 |
Cl- | Na+가 흡수될 때 같은 방향으로 NCC를 통해 흡수 |
Ca2+ | ① Basolateral에서 Na+ gradient 따라 Ca2+ 배출 → 세포 내부의 Ca2+↓ ② Apical에서 Ca2+ channel을 통해 흡수 |
(3) 관련 질환: Gitelman's syndrome
① NCC의 기능 상실
② HypoK/alkalosis(저혈량에 대한 aldosterone↑ 등), hyperCa(세포 내부 Na+↓ → Na+ gradient↑ → Ca2+ 재흡수↑)
(4) 관련 이뇨제: Thiazide
① 원리: NCC 억제 → Na+ 재흡수↓ → 이뇨 작용
② 부작용: HyperCa, hyperuricemia
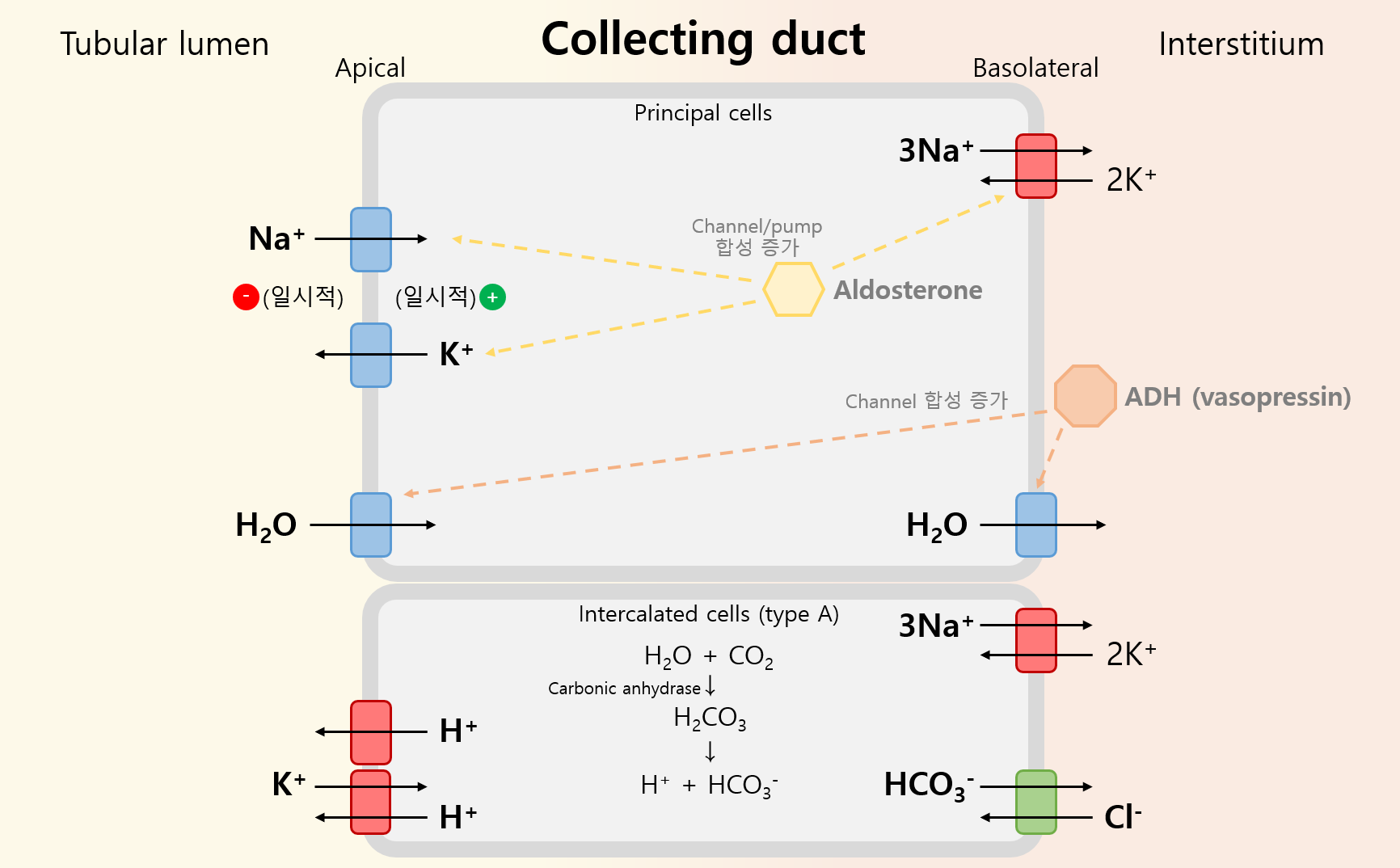
4) 집합관(collecting duct, CD)
(1) 기능
① Principal cells: Na+ 재흡수/K+ 분비 조절(aldosterone), H2O 재흡수 조절(ADH)
② Intercalated cells: 산-염기 평형 조절
• Type A: H+ 분비, HCO3- 재흡수 (acidosis가 있을 때 주된 형태)
• Type B: H+ 재흡수, HCO3- 분비 (alkalosis가 있을 때 주된 형태)
(2) 관련 주요 물질
Na+ | ① Basolateral에서 Na+/K+ pump에 의해 세포 내부의 Na+↓ ② Apical에서 Na+ channel(ENaC)를 통해 흡수 (aldosterone에 의해 항진) |
K+ | ① Na+가 흡수되며 일시적으로 tubular lumen은 (-), 세포 내부는 (+) 전하를 띠게 됨 ② Electrical gradient에 따라 양이온인 K+가 분비됨 (aldosterone에 의해 항진) ③ 분비된 K+ 중 일부는 intercalated cell에서 H+와 교환되어 재흡수 |
H2O | ① Loop of Henle 이후로 H2O는 흡수되지 못함 → lumen은 hypotonic, interstitium은 hypertonic ② H2O channel(aquaporin)을 통해 흡수 (ADH에 의해 항진) |
H+ | ① H2O, CO2가 CA에 의해 H2CO3로 합성 → H+ + HCO3-로 분리됨 ② Acidosis가 있을 때 type A intercalated cell의 apical 쪽에서 H+ pump를 통해 분비됨 ③ Alkalosis가 있을 때 type B intercalated cell의 basolateral 쪽에서 H+ pump를 통해 재흡수됨 |
HCO3- | ① H2O, CO2가 CA에 의해 H2CO3로 합성 → H+ + HCO3-로 분리됨 ② Acidosis가 있을 때 type A intercalated cell의 basolateral 쪽에서 Cl-과 교환되어 재흡수됨 ③ Alkalosis가 있을 때 type B intercalated cell의 apical 쪽에서 Cl-가 교환되어 분비됨 |
(3) 관련 질환: Liddle’s syndrome
① Principal cell의 ENaC의 과활성화
② HTN(Na+ 흡수↑ → 혈장량↑), hypoK(Na+ 흡수↑ → electrical gradient↑ → K+ 분비↑), alkalosis(K+ 분비↑ → H+/K+ 교환↑ → H+ 분비↑)
(4) 관련 이뇨제
① Spironolactone: Aldosterone 억제 → Na+ 재흡수↓, K+ 분비↓ → 이뇨 작용, K+-sparing 효과
② Amiloride, triamterene: ENaC 억제 → Na+ 재흡수↓, K+ 분비↓ → 이뇨 작용, K+-sparing 효과
5. 이뇨제(diuretics)
이뇨제 | 작용 부위 | 원리 | 부작용 |
Acetazolamide | PT | CA 억제 → Na+/H+ 교환↓ → Na+ 재흡수↓ | Renal tubular acidosis |
Loop diruetics | LoH | NKCC 억제 → Na+ 재흡수↓ | HypoCa (+ hypoK, alkalosis) |
Thiazide | DT | NCC 억제 → Na+ 재흡수↓ | HyperCa (+ hypoK, alkalosis) |
Spironolactone | CD | Aldosterone 억제 → Na+ 재흡수↓ | HyperK |
Amiloride | CD | ENaC 억제 → Na+ 재흡수↓ | HyperK |
신장 생리 정리 | ||||
물질 | PT | LoH | DT | CD |
H2O | 재흡수 | 재흡수 | ||
Na+ | 재흡수 | 재흡수 | 재흡수 | 재흡수 |
K+ | 재흡수/분비 | 분비 | ||
Cl- | 재흡수 | 재흡수 | 재흡수 | |
H+ | 분비 | 재흡수/분비 | ||
HCO3- | 재흡수 | 재흡수/분비 | ||
Ca2+ | 재흡수 | 재흡수 | 재흡수 | |
Phosphate | 재흡수 | |||
Glucose | 재흡수 | |||
Harrison 22e, pp.2363-2372