감염병의 역학
이론과 하이라이트 히스토리를 확인 할 수 있어요.
현대에는 의학의 초점이 감염병보다는 만성질환에 맞춰져 있지만, 감염병의 발생에 대한 이해와 관리 원칙은 아직 중요하기 때문에 역학 파트에서 높은 비중을 두고 출제된다. COVID-19가 전세계적으로 창궐하기 시작한 2020년부터 국시와 임종평에서의 출제 빈도가 급격히 늘었으므로 반드시 꼼꼼하게 공부해야 하는 단원이다. 감염 관련 지표를 어떻게 계산하는지, 감염병 관리의 원칙은 무엇이고 감염병의 자연경과와 어떤 관계가 있는지, 기초재생산지수 R0과 집단면역의 계산은 어떻게 이루어지는지에 대해 특히 잘 알아야 한다.
1. 감염병의 감염 경과
1) 발생 모형: 생태학적 모형(병원체, 숙주 환경)
2) 감염 경과
사람 중심으로 보았을 때 | |
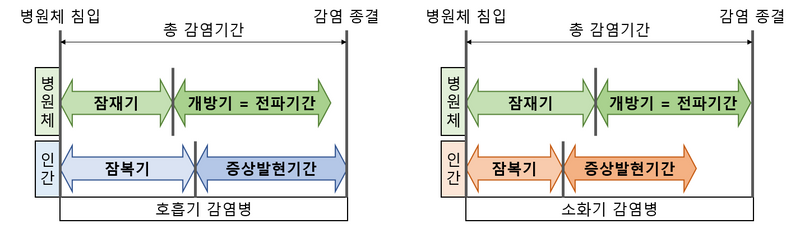
잠복기 Incubation period | • 병원체 침입 ~ 숙주 증상발현까지 • 검역 기간을 설정할 때 고려하는 기간 |
증상발현기간 | • 증상의 발생, 발현, 소실을 거침 |
병원체 중심으로 보았을 때 | |
잠재기 Latent period | • 병원체 침입 ~ 숙주에게서 발견되기 전까지 |
개방기 = 전파기간 Patent period | • 숙주에게서 발견 ~ 더 이상 발견되지 않기까지의 기간 • 이 때 전파가 가능해 전파기간이라고도 함 |
기타 | |
세대기 Generation time | • 병원체 침입 ~ 전염력이 가장 높을 때 • 유행곡선의 peak 사이의 간격 |
연쇄발병간격 Serial interval | • 한 명의 환자, 그 환자로부터 감염된 환자의 발병일 간의 기간 • 세대기의 현실적 산출이 어려울 경우 대체로 시행 |
(1) 호흡기 감염병: 증상 발현 시작 전부터 개방기 시작 → 증상 후 격리에 한계가 있음
(2) 소화기 감염병: 개방기가 증상발현기간보다 늦게 끝남 → 증상이 없어도 격리 필요
* 모든 호흡기/소화기 감염병에 위 내용이 적용되는 것은 아니다.
3) 감염병의 지표
전체 감염 | ||||
불현성감염 (A) | 현성감염 (B+C+D+E) | |||
경미한 증상 (B) | 중등도 증상 (C) | 심각한 증상 (D) | 사망 (E) | |
(1) 감염력(infectivity): 병원체가 숙주에 침입해 질병을 일으키는 능력

(2) 이차발병률(secondary attack rate): 노출된 사람 중 발병하는 비율

* 감염력과 이차발병률의 경우 분모에 ‘감수성 있는 사람’이라는 단서가 중요하다. 만약 과거 감염이나 예방접종에 의한 예방률이 100%라면 과거 감염자, 예방접종자는 분모에서 제외해야 한다. 이차발병률의 경우 일차환자도 제외해야 하는 것 또한 당연하다.
(3) 병원성(pathogenicity): 감염자 중 증상이 발현하는 인원 비율

(4) 독성(virulence)

4) 병원체의 이동
(1) 병원소(reservoir): 병원체(pathogen)가 생존/증식해 숙주에게 전파될 수 있는 곳
① 인간 병원소: 환자(patient), 보균자(carrier, 임상증상 없지만 병원체 있음)
② 동물 병원소: 신종감염병의 발생에 중요한 역할
③ 환경 병원소: 흙, 물, 식물 등
(2) 병원소에서 탈출(exit): 혈액, 기도분비물, 분변, 병변부위 삼출액 등을 통해 탈출
(3) 전파(transmission)
① 직접전파: 피부접촉, 점막접촉, 수직감염, 물림, 비말 등
② 간접전파: 무생물매개(식품, 수인성, 공기 등), 생물매개(모기, 진드기 등)
(4) 새로운 숙주로 침입(entry): 탈출경로, 전파수단과 밀접한 연관성
2. 감염병의 관리와 예방
1) 감염병 관리
(1) 병원소 관리
① 가장 확실한 방법: 병원체 or 병원소의 제거 & 격리
* ex) 결핵균을 항결핵제로 멸균, AI 발생시 해당 양계장의 모든 닭 살처분
② 인간 병원소: 적절한 격리, 치료 → 병원소 수 감소
③ 동물 병원소: 닭, 돼지 등 살처분
(2) 전파과정 관리
① 격리 (isolation) | ② 검역 (quarantine) |
감염자를 감염력이 없어질 때까지 감수성자로부터 분리하는 것 | 국외 감염병이 국내로 유입되는 것을 방지하기 위한 적극적 감시 & 건강 격리 |
대상: 감염자 = 환자 + 보균자 | 대상: 건강하지만 감염 위험성이 있는 사람 |
기간: 감염력이 없어질 때까지 | 기간: 감염 의심 시점 ~ 질병의 최대 잠복기 |
* 검역대상의 조건인 ‘감염 위험성’에 해당하려면 당연히 질병에 대한 감수성이 있어야 한다. 질병에 대한 감수성이 없다고 판단되면(ex. 예방접종자) 검역대상에 포함되지 않을 수 있다.
③ 위생 관리: 환경위생, 식품위생, 개인위생 등
(3) 숙주 관리
① 숙주 면역 증강: 예방접종, toxoid, IVIG, 기타 영양 보조 등
② 환자 조기발견 조기치료
2) 예방접종
(1) 의의: 집단면역을 높여 감수성자가 일상적 접촉에서 감염될 확률을 낮춤
(2) 집단 예방접종의 선정 기준
① 예방접종의 예방효능 및 효과
② 예방접종의 안전성
③ 질병부담 대비 예방접종의 유용성: 자연감염의 해악이 크지 않거나 유병률이 매우 낮을 때
④ 예방접종의 cost-benefit
⑤ 예방접종 방법의 용이성: DTaP, MMR과 같은 혼합백신 사용
(3) 백신 효과(vaccine efficacy): 접종군과 비접종군의 발생률을 비교

3) 전염병 감시 체계
(1) 수동감시체계: 평시에 운영, 법정 감염병에 대한 신고 기반
• 편리한 운영 / 보고의 낮은 완전성
(2) 능동감시체계: 전염병의 유행시 운영, 정보를 능동적으로 수집
• 높은 완전성 / 높은 비용, 시간, 인력 필요
3. 유행과 면역
이론부터 문제까지, 알렌의 서재를 100% 활용하세요
※ 로그인 후 이용권 구매 시 전체 이용 가능합니다.
6,000개 이상의 문제와 연결되는 이론으로 개념과 적용을 한 번에
실제 국시와 동일한 CBT 환경으로 실전 감각 완성
틀린 문제를 매일 자동으로 챙겨주는 ‘오늘의 문제’
메모·암기카드·노트로 만드는 나만의 복습노트
커뮤니티 Q&A
위 이론과 관련된 게시글이에요.
메트로니다졸리다
26.05.02
세대기
이론부분에 보면 세대기는 1) 병원체 침입 ~ 전염력이 가장 높을 때 2) 유행곡선의 peak 사이의 간격이라고 설명되어 있습니다. 3) 근데 또 문제 풀다보면 여러번의 bump가 있을 때 세대기는 첫 발생인 3/7부터 두 번째 발생 peak인 3/...
조회수 50
댓글 3
추천수 0
메트로니다졸리다
26.05.02
310
25.12.24
전파 vs 숙주관리
전파관리과정 3번 위생 관리에서 개인위생이랑 숙주관리랑 무슨 차이인가요..?
조회수 134
댓글 1
추천수 1
310
25.12.24
공부시작했다공부끝났다
25.11.22
인간의 격리는 병원소 관리인가요 전파과정 관리인가요?
병원소 관리 중 “인간 병원소 : 적절한 격리, 치료 → 병원소 수 감소” 가 있고, 전파과정 관리에도 격리가 있네요 ㅜㅜ ....
조회수 222
댓글 3
추천수 0
공부시작했다공부끝났다
25.11.22