역학적 연구 방법
이론과 하이라이트 히스토리를 확인 할 수 있어요.
역학에서 가장 많은 문항들에 출제되는 부분 중 하나이기 때문에 각 연구방법이 언제 사용되는지, 한계는 무엇인지, 관련해서 도출할 수 있는 통계적 지표가 무엇이고 어떻게 계산하는지에 대해 빠짐없이 알고 있어야 한다.
1. 분류
1) 관찰연구(observational study)
(1) 정의: 질병의 원인과 결과에 직접 개입하지 않고 관찰을 통해서 인과관계를 밝히는 연구
(2) 기술역학연구
① 질병 발생의 양상을 시간적, 공간적, 인적 특성에 따라 기술하는 연구 방법
② 인과 관계를 보일 수는 없음
③ 예시: 사례연구, 사례군 연구, 생태학적 연구, 단면연구
(3) 분석역학연구
① 가설을 설정하고 비교군을 제시하고 질병 발생의 차이를 분석하는 방법
② 인과 관계를 보일 수 있음
③ 예시: 환자 대조군 연구, 코호트 연구, 단면연구
2) 실험연구(experimental study)
(1) 정의: 질병의 원인을 연구자가 직접 결정하거나 변화시키는 연구
(2) 무작위배정 등을 통해 연구 조건들을 배정/통제해 바이어스를 최소화하는 형태
(3) 예시: 무작위 임상 시험, 지역 사회 시험
3) 인과성에 대한 근거 수준: 아래로 갈수록 근거 수준이 높음
(1) 사례연구, 사례군 연구
(2) 생태학적 연구
(3) 단면연구
(4) 환자-대조군연구
(5) 코호트연구
(6) 준실험연구
(7) 실험연구
2. 기술역학의 세 주요 변수(TPP)
1) 시간(T, time)
(1) 장기 추세 변동: ex) 꾸준히 유병률이 감소하고 있는 폐암
(2) 주기변동: ex) 홍역처럼 몇 년을 주기로 집단으로 발병하는 감염질환
(3) 계절 변동: ex) 겨울의 influenza, 가을의 쯔쯔가무시 등
(4) 유행곡선: 감염질환 outbreak 때 짧은 시간 단위로 질병 발병건수 기록
2) 공간(P, place)
(1) 지역응집성: 응집성의 수준에 따라 산발성, 풍토병, 유행병, 범유행병으로 분류
(2) 지역 간 비교 단위
① 지역 분포 비교: 점지도(spot map)를 이용해 감염원, 감염경로를 확인
ex) 19세기 John Snow가 런던 콜레라의 점지도를 이용해 수도시설을 원인으로 지목함
② 지역 간 비교: 도시-농촌, 시군구별, 시도별 비교에 사용
③ 국가 간 비교
3) 사람(P, person)
(1) 연령: 질병 발생과 사망에 가장 영향력이 큰 변수
(2) 성별: 대다수의 질병에서 대체적으로 남자가 여자보다 사망률이 높음
(3) 결혼 상태: 기혼자의 사망률이 낮음
(4) 직업, 사회경제적 수준, 가족 관계, 유전적 감수성, 인종, 종교 등
3. 사례연구(case study), 사례군연구(case series study)
1) 사례연구: 기존에 보고되지 않은 특이한 질환 양상을 보이는 단일 환자에 관한 기술
* ex) 젊고 건강했던 남성이 Pneumocystis 폐렴(PCP)에 걸린 현상을 보고
(1) 한계: 인과성 확립과 발생수준 측정은 불가능
(2) 의의: 새로운 연구의 촉매제로서의 기능
2) 사례군연구: 사례연구에 해당하는 사례들의 공통점을 기술해 가설을 설립
* ex) 젊고 건강했던 남성 5명이 PCP에 걸림 → 5명 모두 동성애자라는 공통점 발견 → 동성애 관련 행태가 면역저하를 유발한다고 추론 (AIDS의 첫 보고)
(1) 한계: 대조군이 없어 인과성을 밝힐 수는 없음
(2) 의의: 기존에 밝혀지지 않았던 새로운 인과성에 대한 가설 제시가 가능해짐
4. 생태학적 연구(ecological study)
1) 인구집단을 관찰 단위로 해서 기존에 생성된 자료를 바탕으로 상관 분석을 진행하는 연구
* ex) 각국의 미세먼지 농도와 결핵 유병률에 관한 자료를 얻어 둘 사이의 연관성을 분석
2) 장점
(1) 자료 수집과 분석의 간편성, 신속성, 경제성
(2) 환경오염과 같이 개인 수준의 노출 측정이 어려운 변수 연구에 적합
3) 단점
(1) 생태학적 오류(ecological fallacy)
① 분석 단위가 개인이 아닌 집단이므로 집단에서 발견된 연관성과 실제 개인 단위에서의 연관성이 다를 수 있음
② 따라서 집단 수준의 연관성이 있어도 개인 수준에 그대로 적용할 수는 없음
* ex) 미세먼지 농도가 높은 나라일수록 결핵의 유병률이 높음 → 하지만 개인이 미세먼지에 노출될수록 결핵 발병 가능성이 높아진다고 말할 수 없음
(2) 자료의 불완전성, 원인적 요인과 질병 발생간의 불투명한 선후관계
5. 단면연구(cross-sectional study)
1) 질병의 유병 여부와 위험요인 노출 정보를 하나의 같은 시점에 얻어 연관성을 분석
* ex) 의대생의 현재 성적과 현재 우울증 척도 점수를 동시에 설문한 후 연관성을 분석
2) 장점
(1) 유병률 조사에 유리함
* ex) 위 조사는 의대생의 현재 우울증 시점유병률만을 조사하는 데는 적합한 연구설계
(2) 연구 설계가 간단하며, 기간이 짧고 경제적임
(3) 응답률이 높음: 한 번만 응답하면 되기 때문
3) 단점
(1) 시간적 선후관계 정보가 없어 인과관계 규명이 매우 어려움
* ex) 만약 의대생의 우울증 척도 점수가 높을수록 성적이 낮다면, 의대생이 우울해서 성적이 낮은 것인지 성적이 낮아 우울한 것인지 명확하지 않음
(2) 선택적 생존 바이어스 가능: 현재 살아남은 사람만 연구에 포함되기 때문
* ex) 극심한 우울로 인한 휴학, 자퇴, 제적은 조사에 반영되지 못함
(3) 희귀한 질환이나 이환 기간이 짧은 질병은 적합하지 않음
* ex) 우울 대신 현재 환청 여부를 묻는다면 유병률이 0일 가능성이 매우 높음
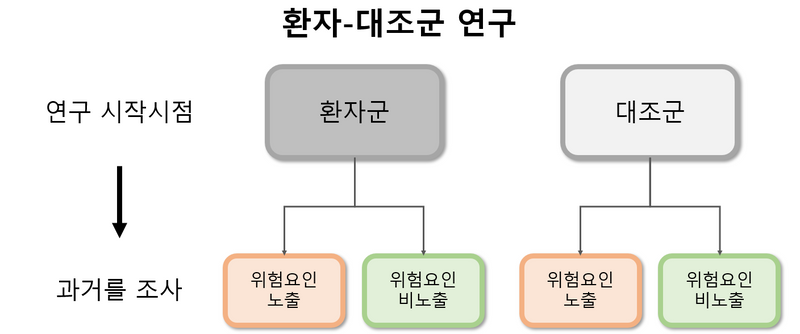
6. 환자-대조군 연구(case-control study)
1) 현재 환자(case)와 대조군(control)을 추출해서 두 집단의 과거의 위험요인 노출력을 후향적으로(retrospective) 비교해 연관성을 분석
* ex) 흡연과 SLE 발생 사이의 연관성을 분석하기 위해 현재 SLE로 치료중인 환자와 일반인 대조군을 추출하고, 각 집단에게 흡연력에 대해 설문해 비교함
2) 장점
* 환자-대조군 연구의 장단점은 아래 코호트 연구의 장단점과 대응되는 부분이 많다.
(1) 작은 표본으로도 연구 가능 → 적은 비용
(2) 단기간에 연구 수행 가능
(3) 희귀질환, 잠복기가 긴 질환에 대한 연구에 적합
(4) 한 번에 여러 위험요인에 대해 설문해 효율적인 분석 가능, 적은 윤리적 위험 등
3) 단점
(1) 시간적 선후 관계가 불분명함 → 인과성 낮음 & 비교위험도 계산 불가능
* ex) 환자에 따라 흡연과 SLE 중 무엇이 더 먼저 발생했는지 불분명한 경우가 많음
(2) 드물게 노출되는 위험요인에 대한 연구에 부적합
(3) 선택 바이어스: 적절한 대조군을 선택하기 어려움
(4) 정보 바이어스(특히 기억 바이어스): 과거 노출력에 대한 정보가 기억에 의존할 때
* ex) ‘흡연’에 대한 정보는 환자의 기억에 의존해야 할 때가 대다수인데, SLE 환자는 일반인보다 스스로의 옛 생활습관을 더 잘 기억할 가능성이 높음
(5) 통제가 필요한 변수에 대한 정보를 얻지 못할 수 있음
4) 대조군의 선정: 환자-대조군 연구에서 가장 중요한 부분
(1) 환자군과 여러 특성이 유사하면 이상적임 (연령, 성별, 인종, 사회경제적수준 등)
(2) 환자군, 대조군 모두 동일한 방법으로 과거 노출력에 대한 정보를 얻어야 함
(3) 교란변수의 최소화: 짝짓기(matching)
① 예상되는 몇 가지 교란변수를 설정: 보통 2~3개
* 너무 많은 교란변수를 통제하려고 하면 효과적인 짝짓기가 불가능해진다.
② 환자군 개개인마다 해당 교란변수가 완전히 같은 사람을 대조군에서 추출
* 환자군의 한 사람마다 대조군에서 한 사람을 1:1 대응(개별 짝짓기)시키지 않고, 환자군과 대조군 전체에서 교란변수의 분포라 동일하도록 하는 방식(빈도 짝짓기)도 존재한다.
5) 교차비(비차비, 오즈비, odds ratio, OR)
(1) 환자-대조군 연구는 다음 이유로 비교위험도를 계산할 수 없음
① 시간적 선후관계가 명확하지 않음
② 환자군과 대조군의 비를 연구자가 설정함
(2) 따라서 비교위험도에 대한 대체치로 OR을 계산
환자군 (ex. SLE 환자) | 대조군 (ex. 일반인) | |
위험요인 노출 (ex. 흡연력 있음) | a | b |
위험요인 비노출 (ex. 흡연력 없음) | c | d |
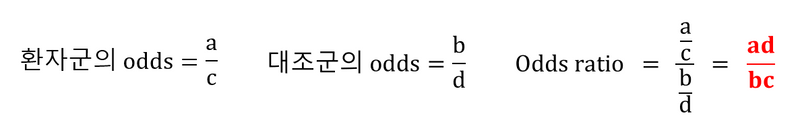
• 유병률이 낮을수록 OR과 비교위험도는 같아짐
(3) 짝짓기를 시행했을 경우 OR 계산
짝지은 쌍에 대한 교차표 | 대조군 | ||
요인 노출 있음 | 요인 노출 없음 | ||
환자군 | 요인 노출 있음 | a | b |
요인 노출 없음 | c | d | |
* 표를 읽는 법이 헷갈릴 수도 있는데, 위 표의 a, b, c, d는 짝지어진 (환자군, 대조군)의 개수다. 예를 들어 a = 20이면 짝지어진 여러 (환자군, 대조군) 쌍 중 환자군과 대조군 모두 요인 노출이 있었던 쌍이 20쌍이라는 뜻이다.

* 하지만 성별이나 나이처럼 단순한 변수에 대해 짝짓기가 이루어진 경우 일반적인 방법대로 ad/bc로 계산할 수도 있다.
7. 코호트 연구(cohort study)
1) 위험요인에 노출된 집단과 비노출된 집단을 추적관찰하여 두 집단의 질병 발생을 비교해 연관성을 분석
* ex) 부모의 흡연 여부와 소아 천식의 발생 사이의 연관성을 분석하기 위해 흡연자 부모에게 태어난 아기와 비흡연자 부모에게 태어난 아기를 최대 18년간 추적관찰해 비교함
2) 분류
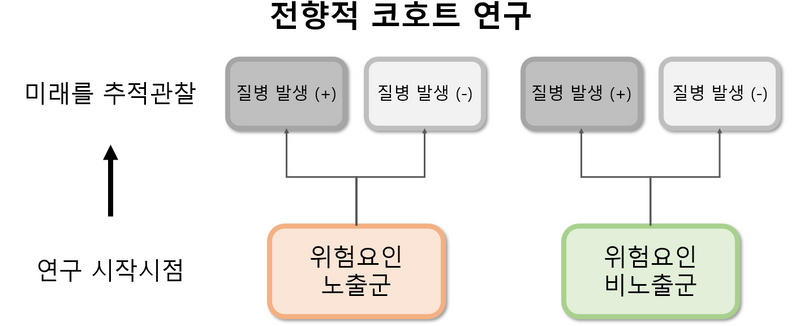
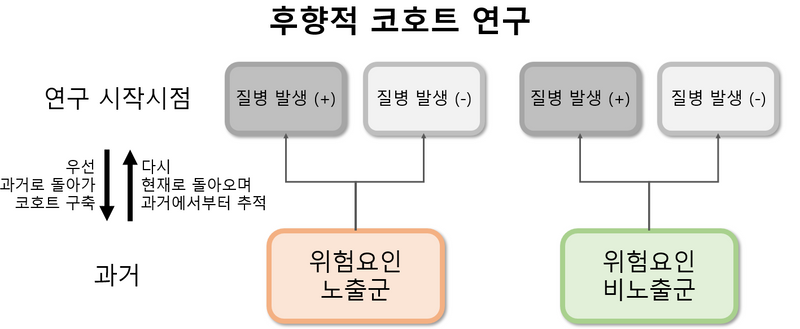
전향적 코호트 (prospective cohort) | 후향적 코호트 (retrospective cohort) |
연구자가 먼저 코호트를 직접 구축 | 과거의 자료를 토대로 코호트를 구축 |
이후 수 년을 직접 추적관찰 후 연구 종료 | 과거의 자료를 토대로 노출 정보를 추적 |
장점 | |
연구 목적에 최적화된 코호트 구축 가능 | 낮은 비용/시간 |
단점 | |
높은 비용/시간 | 본 연구 목적의 데이터가 아님 제한적인 설명변수 설명변수를 1번밖에 측정하지 못함 관찰하고자 하는 질병이 이미 발생함 |
* 전향적 코호트 연구의 가장 큰 단점인 ‘높은 비용과 시간’을 회피하기 위해 데이터의 완전성과 연구의 유연성을 일부 희생한 것이 후향적 코호트라고 생각하면 된다.
3) 코호트 연구의 장점
(1) 시간적 선후 관계가 비교적 분명함 → 인과성 높음 & 비교위험도 계산 가능
(2) 노출과 수많은 질병간의 연관성을 볼 수 있음
(3) 위험요인에 노출된 시기부터 질병이 발생하기까지 전 과정 관찰 가능
(4) 위험요인 노출 수준을 여러 번 측정 가능
4) 코호트 연구의 단점
(1) 높은 비용과 시간 (후향적 코호트 연구는 이를 회피함)
(2) 추적관찰 탈락에 의한 바이어스
(3) 시간에 따라 노출 상태나 진단검사법, 진단기준 등이 변화할 수 있음
(4) 희귀질환에 대해 연구하기 어려움
5) 분석
(1) 발생률(incidence): 코호트 연구에서만 계산 가능
질병 발생 (+) | 질병 발생 (-) | 발생률 | |
위험요인 노출군 | a | b | a / (a+b) |
위험요인 비노출군 | c | d | c / (c+d) |
(2) 비교위험도(상대위험도, relative risk, RR): 두 발생률의 비

① RR > 1: 노출되면 노출되지 않을 때에 비해 RR배만큼 발생률이 높아짐
* 이를 risk factor라고 부른다.
② RR < 1: 노출되면 노출되지 않을 때에 비해 RR배만큼 발생률이 낮아짐
* 이를 protective factor라고 부른다.
③ 통계적 유의미성: RR이 1보다 크건 작건간에 신뢰구간이 1을 포함하지 않아야 통계적으로 유의미한 RR임
ex1) RR = 1.38, 95% 신뢰구간 [0.95, 1.81]이면 신뢰구간 안에 1이 포함되므로 통계적으로 유의미하지 않음
ex2) RR = 1.38, 95% 신뢰구간 [1.04, 1.72]이면 신뢰구간 밖에 1이 있으므로 통계적으로 유의미함
(3) 기여위험도(기여위험분율, attributable risk, AR)

① 노출군의 질병의 발생률에 특정 위험요인이 몇%나 기여했는지 측정
② 해당 위험요인을 제거하면 노출군에서 기여위험도의 %만큼 예방됨
(4) 지역사회 기여위험도(인구집단 기여위험분율)

* P = 위험요인 노출분율
① 지역사회 전체의 질병의 발생률에 특정 위험요인이 몇%나 기여했는지 측정
② 해당 위험요인을 제거하면 지역사회에서 지역사회 기여위험도의 %만큼 예방됨
③ 유병률이 증가하면 지역사회 기여위험도도 같이 증가함
* 문제에서 ‘노출군’의 질병 발생에 대해서 묻는지, ‘지역사회 전체’의 질병 발생에 대해서 묻는지 확실히 파악해야 한다. 전자는 기여위험도, 후자는 지역사회 기여위험도를 계산하면 된다.
8. 혼합설계연구
1) 코호트연구와 환자-대조군연구의 혼합설계
(1) 필요성: 이미 만들어진 코호트 내에서 희귀질환을 연구할 때
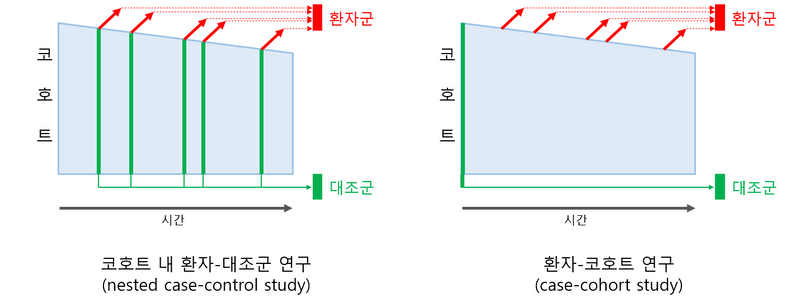
(2) 코호트 내 환자-대조군 연구(nested case-control study)
① 코호트 내에서 환자가 발생할 때마다 즉시 대조군도 하나 추출함
② 이 때 대조군은 환자의 특성에 맞게 짝짓기되어 추출될 수 있음
③ 환자들과 대조군 구성원들은 각자 추출될 당시의 정보를 바탕으로 각각 환자군, 대조군을 이룸
④ 환자군과 대조군이 만들어지면 환자-대조군 연구 수행
(3) 환자-코호트 연구(case-cohort study)
① 미리 처음부터 대조군 기능을 할 서브코호트(subcohort)를 추출하고 시작
② 이후 코호트 내에서 환자가 발생하고, 당시의 정보를 바탕으로 환자군 형성
③ 서브코호트를 대조군 삼아 환자-대조군 연구 수행
(4) 공통적 장점
① 회상 바이어스 극복: 이미 코호트 내에서 확보된 정보와 검사결과가 존재
② 시간적 선후관계 명확: 이전에 코호트에서 확보한 시료를 현재와 대조 가능
③ 연구의 높은 효율성
2) 환자-교차설계 연구(case crossover design)
(1) 환자 스스로를 대조군으로 이용하는 연구
(2) 환자군: 사건이 발생하기 직전
(3) 대조군: 사건이 발생하지 않았던 시기
(4) 조건
① 노출부터 질병발생까지의 기간이 짧아야 함
② 위험 요인 노출의 효과가 일시적이고 금방 사라져야 함
3) 패널 연구(panel study)
(1) 단면 연구와 코호트 연구의 혼합
(2) 단면연구를 했던 대상(패널)을 추적 관찰하면서 변화 추이를 관찰
9. 임상시험(clinical trial)
1) 새로 개발한 진단법/치료법 등을 사람에게 적용 후 그 안전성과 효능을 평가하는 실험역학연구
(1) 장점: 근거 수준이 가장 높은 연구방법
(2) 단점: 윤리적, 시간적, 비용적 문제
2) 임상시험의 단계
대상 | 목적 | 대상자 수 | |
전임상 (preclinical) | 동물 | 약물의 효능/안전 확인 | 다양 |
1상 (phase I) | 일반인, 환자 | 약동학, 투여용량 상한선 확인 | 5~20 |
2상 (phase II) | 환자 | 최적 투여용량 결정, 치료효과 탐색, 중대한 부작용 탐색 | 30~100 |
3상 (phase III) | 환자 | 안전성, 유효성 검증 | 100~1000 |
4상 (phase IV) | 환자 | 부작용 추적관찰, 다른 질환에 대한 약물 효과 탐색 | > 3상 |
3) 설계
(1) 평행설계(parallel design)
① 연구대상자 모두에게 screening 기간동안 위약투여 → 기존 약물 체내 소실
② 대상자를 두 개 이상의 군으로 무작위배정
③ 각 군은 한 가지 치료법만 적용받음
(2) 교차설계(crossover design)
① 대상자를 두 개 이상의 군으로 무작위배정
② 한 군은 치료법 A, 다른 군은 치료법 B를 일정 기간 적용
③ 이후 치료법 A를 받았던 군에게는 치료법 B를, 다른 군은 반대로 동일한 기간 적용
④ 고려사항
• 잔류효과(carry-over effect): 치료법을 바꿀 때 새 치료법이 이전 치료법과 상호작용하는 현상
• 휴약기간(washout period): 잔류효과를 막기 위해 아무것도 투여하지 않는 기간
• 교차설계가 부적절한 질병: 환자 상태가 비가역적으로 악화되거나, 주기적으로 호전과 악화를 반복하는 질병
4) 비교군 설정
(1) 표준치료가 존재할 경우: 새로운 치료제 군을 표준치료제 군과 비교
* 표준치료제가 존재함에도 치료하지 않거나 위약을 쓰것은 비윤리적이다.
(2) 표준치료가 없을 경우: 새로운 치료제 군을 위약군, 무치료군과 비교
① 위약(placebo)군: 치료효과가 통증개선, 인지기능 개선 등 주관적일 때
② 무치료군: 위약을 비윤리적 이유 등으로 쓸 수 없을 때 (침습적 시술 등)
5) 시험대상자 수 산출
(1) 지나치게 적을 경우: 통계적 검정력이 낮아져 가설에 대한 타당한 검증이 불가
(2) 지나치게 많을 경우
• 비용이 과대해짐
• 필요 이상의 피험자를 부작용의 위험에 노출시키는 것은 비윤리적
6) 무작위배정법(randomization)
(1) 대상자 중 누가 치료군, 누가 비교군에 들어가는지를 무작위로 결정하는 것
(2) 두 군 사이의 비교성을 극대화할 수 있음
(3) 윤리적으로 가장 타당하며, 통계적 분석의 기본 조건을 만족시킴
7) 눈가림법(blinding)
(1) 특정한 대상자가 치료군인지 비교군인지 알지 못하게 하는 것
(2) 양측눈가림법(double blinding): 피험자, 의사 모두 모르기 때문에 위약효과나 의사의 비의도적 조작(unintentional intervention)을 예방
8) 기타 고려사항
(1) 윤리 준수: 충분한 설명을 들은 후의 자발적 동의(informed consent) 등
(2) 연구대상 선정
① 일반화가 가능하도록 대표성이 있어야 함
② 치료에 대한 순응도가 높고 추적조사의 가능성이 높아야 함
(3) 치료효과에 대한 객관적 확인이 가능해야 함
(4) 치료결과의 판정을 언제, 어떤 기준으로 할 것인지 신중히 결정해야 함
(5) 치료효과를 중간결과로 평가할 경우 그 기준을 신중이 결정해야 함
(6) 연구자료의 수집과 데이터베이스 구축을 어떻게 완전하게 수행할지 결정해야 함
(7) 연구자료의 통계적 분석을 어떤 방법으로 할지 사전에 결정해야 함
(8) 환자당 연구비를 최소화해야 함
10. 기타 연구 방법
1) 예방시험(preventive trial): 위험성이 비교적 적은 약제나 예방법을 통해 질병 발생이 감소함을 확인하는 연구
2) 지역사회시험(community trial): 지역사회 구성원을 대상으로 각종 보건/예방사업의 효과를 평가하기 위한 연구
3) 메타분석(meta-analysis): 기존의 적합한 연구결과들을 통합적으로 분석/제시하는 연구 (출판 바이어스 주의 필요)
4) 이민자 연구: 환경과 유전의 상대적인 중요성에 대한 연구
5) 쌍둥이 연구: 유전적 동질성이 질병 발생에 어떠한 영향을 주는지에 대한 연구
6) 출생코호트 연구: 노령인구에서의 발생률이나 사망률이 생물학적 특성과 다르게 감소하는 현상이 발견될 때 필요한 연구
예방의학과 공중보건학 제4판, pp.169-239