효소
이론과 하이라이트 히스토리를 확인 할 수 있어요.
매년 한두 문제씩 출제되는 부분으로, 미하엘리스-멘텐 식과 효소의 억제제에 관한 이해를 묻는 문제들이 나온다. 특히 효소의 억제제를 그 기전에 따라 구분하여 이해하는 것이 중요하다.
1. 효소의 개념
1) 정의: 생리작용의 반응 속도를 조절하는 생체촉매
2) 작용 기전: 반응의 활성화 에너지를 감소시켜 (ΔG‡uncat > ΔG‡cat) 평형에는 영향 없이 속도 변화
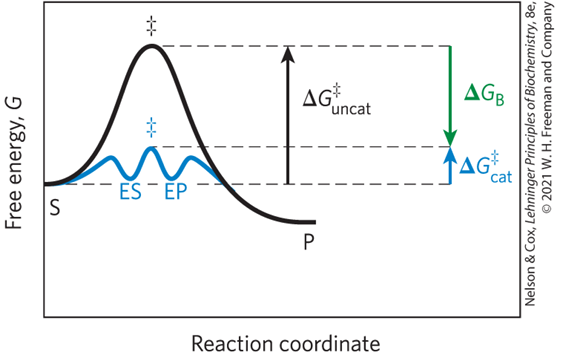
3) 전이상태: 화학 반응 과정 중 나타나는 에너지가 높은 상태, 효소는 전이상태의 기질과 상보적으로 결합해 효소-기질 복합체 형성
2. 미하엘리스-멘텐 방정식(Michaelis-Menten Equation)
1) 공식:
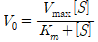
2) 그래프
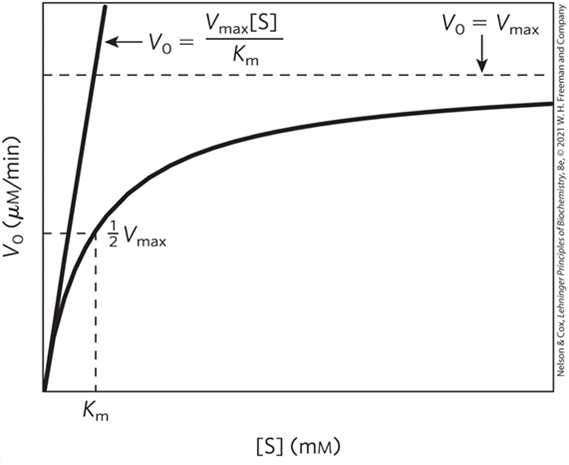
(1) [S]-V0 그래프
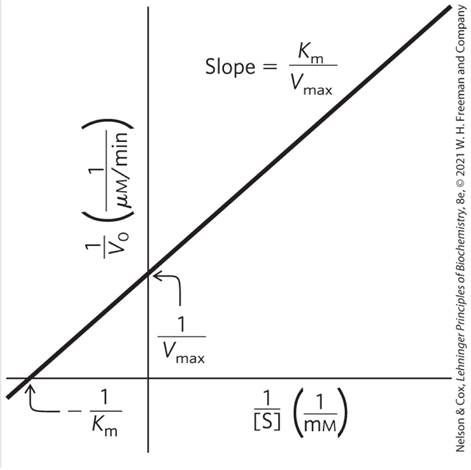
(2) 이중역수도표(라인위버-버크 도표)
• 공식
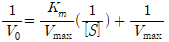
3) Km: 초기 반응 속도가 Vmax/2가 되게 하는 기질의 농도
Km | Affinity(기질 친화도) | Capacity(결합 용량) | 설명 |
↓ | High | Low | 적은 기질 농도로도 Vmax에 빠르게 도달 |
↑ | Low | High | 효소의 포화를 위해 많은 기질 필요 |
• 다중단계 반응에서는 Km이 가장 큰 과정이 속도 결정 단계
3. 효소의 저해
1) 가역적 저해(Reversible inhibition)
(1) 경쟁적 저해(Competitive inhibition)
• 방식: 효소의 기질 결합 부위와 결합
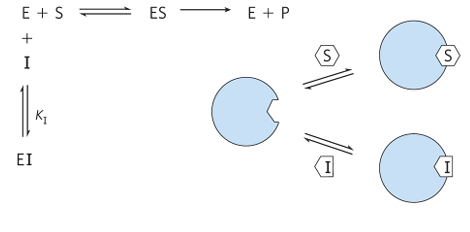
• 특징: 효소와 기질의 구조적으로 유사
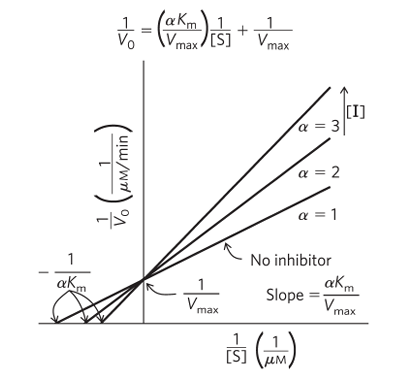
• 라인위버-버크 도표
• 저해제가 증가할 때 (α 증가로 표현됨)
- Km: 증가 (∵ 저해제에 의해 효소의 기질과의 친화력 감소)
- Vmax: 일정 (∵ 기질이 저해제보다 매우 많을 때 저해제 효과 무시 가능)
(2) 비경쟁적 저해(Uncompetitive inhibition)
• 방식: 효소-기질 복합체와 결합
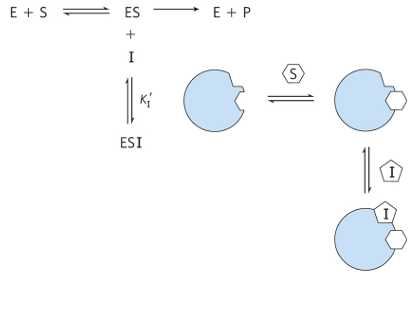
• 특징: 효소의 기질 결합 부위가 아닌 다른 부위와 결합, 효소-기질 복합체가 생성물로 변하는 것을 억제
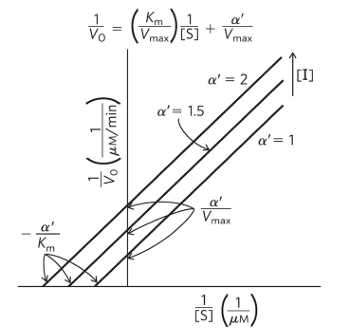
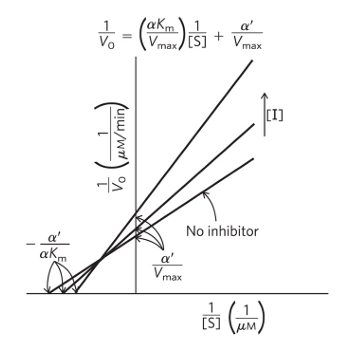
• 라인위버-버크 도표
• 저해제가 증가할 때 (α‘ 증가로 표현됨)
- Km: 감소
- Vmax: 감소
- Km/Vmax (기울기): 불변
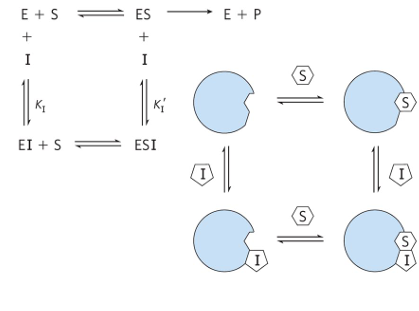
(3) 혼합 저해(Mixed type inhibition)
• 방식: 효소 또는 효소-기질 복합체와 결합
(E: 효소, S: 기질, I: 저해제, P: 생성물)
• 특징: 경쟁적 저해제와는 달리 효소의 기질 결합 부위가 아닌 다른 부위에 결합
• 라인위버-버크 도표
• 저해제가 증가할 때
- Km: 경우마다 다름 (∵ 경쟁적 저해의 효과로는 증가, 비경쟁적 저해의 효과로는 감소)
- Vmax: 감소 (∵ 경쟁적 저해의 효과로는 유지, 비경쟁적 저해의 효과로는 감소)
2) 비가역적 저해(Irreversible inhibition)
4. 효소의 조절(Enzyme regulation)
1) 질적 조절(Regulation by quality)
(1) Allosteric regulation
• Allosteric regulator가 효소의 결합 부위가 아닌 다른 자리(allosteric site)에 붙어 효소의 구조적 변화 유도
• 예시: Feedback inhibition; 대사의 최종산물이 대사 효소를 allosteric inhibition
(2) Covalent modification
• 예시: phosphorylation(m/c), methylation, uridylylation, adenylation
(3) Zymogen activation
• zymogen: 비활성 상태의 효소 전구체
• 효소가 필요한 특정 상황에서만 zymogen이 잘리며 효소 기능 활성화
• 예시: 소화 효소, 보체, caspase
2) 양적 조절(Regulation by quantity)
(1) Gene expression
(2) Enzyme degradation by proteolysis
5. Isozyme
1) 정의: 같은 화학반응을 촉매하는 서로 다른 효소
2) 특징: 서로 다른 아미노산 서열, 서로 다른 Km, Vmax
Reference
• Lehninger Principles of Biochemistry 8th ed, pp. 726~885