항암제
이론과 하이라이트 히스토리를 확인 할 수 있어요.
항암제의 표적과 내성이 생기는 기전을 물어보는 문제들이 주로 출제된다. 항암제 전반의 부작용과 대처 방안, 항암제의 구분법에 대해서도 살펴보고 넘어가는 것이 좋겠다.
1. 항암제
1) 세포사멸 항암제(Cytotoxic drug): 암세포 사멸, 종양 크기 줄임
(1) 화학 항암제
• 기전: 암세포의 빠른 증식(유전자 합성, 세포분열) 억제
• 단점: 비특이적
2) 세포 성장 억제 항암제(Cytostatic drug): 암의 진행 억제
(1) 표적항암제
• 기전: 종양 특이적 표적에 선택적으로 작용
• 단점: 표적 유전자의 변형 등으로 인한 내성
(2) 면역항암제
• 기전: 암세포의 면역 세포 공격을 막거나, 면역 세포의 작용을 도움
• 단점: 과도한 면역으로 인한 자가면역질환
3) 평가 기준
| 세포사멸 항암제 | 세포 성장 억제 항암제 |
작용기전 | 세포사멸 | 종양의 진행 정지 |
효능검색 | 반응율 | 진행율 |
용량 결정 | 최대 내약 용량 | 최대 표적 억제 용량 |
약제 효과 | 종양 축소, 완치율 | 생존 기간, 무진행 기간, 증상 완화, 삶의 질 |
2. 세포독성항암제
1) 세포주기
① G1기: DNA 합성에 필요한 효소, RNA 합성
② S기: DNA 복제
③ G2기: 세포분열을 준비하며 분열에 필요한 물질 합성
④ M기: 세포분열 진행, 이후 다시 G1기나 G0기(휴지기)로 진행
2) 세포주기 특이적 세포독성항암제
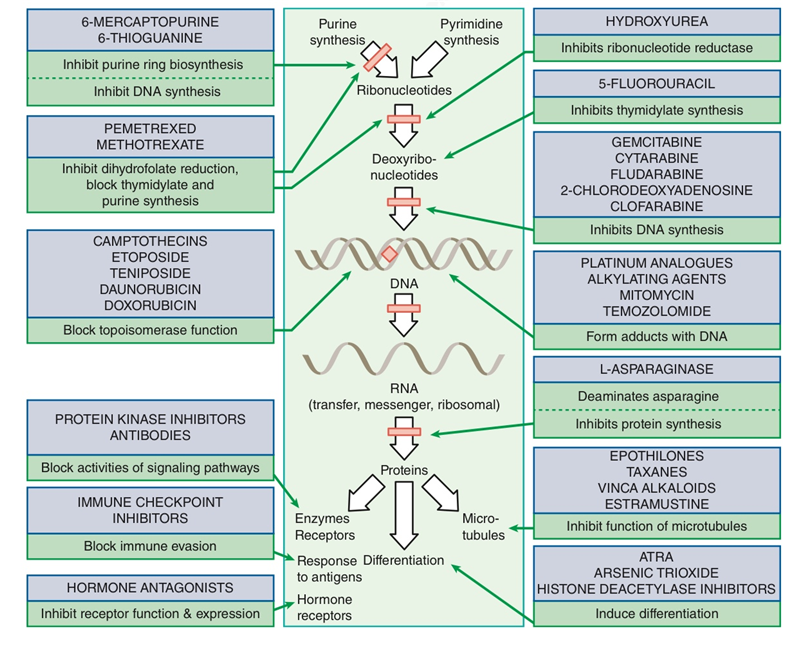
(1) 항대사 항암약물 (S기): methotrexate, hydroxyurea, nucleoside analogues(ara-C, fludarabine, gemcitabine, 6-mercaptopurine), 5-fluorouracil(5-FU), capecitabine, cladribine, cytarabine, nitrosourea, nelarabine, 6-thioguanine, pralatrexate, pemetrexed
• methorexate: dihydrofolate reductase 억제
• hydroxyurea: ribonucleotide reductase 억제
• nucleoside analogues(mimetics): DNA 합성 방해
• 5-fluorouracil: thymidylate 합성 억제, T대신 들어가는 nucleosie 유사체로도 작용
(2) 항생제 항암약물 (G2/M기): bleomycin
(3) Topoisomerase inhibitor (S/G2기): DNA ligation 억제
• Topoisomerase I inhibitor(Camptothecin): irinotecan, topotecan
• Topoisomerase II inhibitor: etoposide, temiposide, anthracycline(adriamycin)
(4) Tubulin 결합 약물 (M기)
• Vinca alkaloid류; tubulin polymerization 억제: vincristine, vinblastine, vinorelvine
• Taxane류; tubulin depolymerization 억제: carbazitaxel, docetaxel, paclitaxel
3) 세포주기 비특이적 세포독성항암제
(1) 알킬화 항암약물: mitomycin-C, busulfan, carmustine, cyclophosphamide, mechlorethamine, melphalan
• DNA의 친핵성 그룹과 공유결합 형성해 DNA 합성 억제(DNA unwinding), 구조 이상 유도
(2) 항생항암약물: dactinomycin, mitomycin
(3) Anthracycline: daunorubicin, doxorubicin, epirubicin, idarubicin
• anthracycline의 경우 topoisomerase II을 억제하기는 하나, 세포주기 전반에 작용할 수 있어 세포주기 비특이적 세포독성항암제로 분류하는 편
(4) 백금 유사 항암약물: carboplatin, cisplatin, oxaliplatin
• nucleotide(주로 G)와 결합해 DNA 구조에 끼어 들어가 DNA 합성 억제, DNA 구조 이상 유도
4) 한계
(1) 저항성, 내성, 부작용
(2) 항암효과의 개인차↑, 사전 치료 경과 예측 어려움
(3) 종양의 개별특성 반영 X
2. 표적항암제
1) 사용: Driver oncogene이나 다른 표적 대상이 있는 경우
2) 방법: 항체를 통해 표적 수용체 억제, 저분자 물질을 통해 표적 물질과 결합해 억제
저분자물질 | 단일클론항체 | |
크기 | 작음 • 세포 내 침투 가능 • 세포 안팎 모두에서 작용 가능 • 주로 경구투여 | 큼 • 세포 내부 침투 불가능 • 주로 세포 밖에서 작용 • 주로 주사를 통해 투여 |
명칭 | -nib | -mab |
표적 단백질 수 | 한 개의 약제가 여러 단백질 표적 (동일 domain 갖는 여러 protein) | 주로 한 개의 약제가 한 단백질 표적 (항원-항체 반응 예외) Aflibercept |
항암제와의 Synergy | 일반적으로 X | 일반적으로 상승효과 |
기타 특징 | ① 기존 항암치료 저항성 가진 암종서 효과 ② 유전자의 돌연변이 특성에 따라 치료 효과 달라짐 ③ 표적치료제에 내성(3차원 구조변화) 생긴 경우 같은 단백질 다른 domain으로 새 표적치료제 개발 가능 | ① 방사성동위원소, 항암제, 독성물질을 운반하는 약제운반체로 개발 가능 ② 세포표면 공격과 동시에 면역반응(ADCC, CDC) 유발, 세포사멸 촉진 가능 ③ 세포독성 항암제, 방사선치료와 병용 시 상승효과 가능 |
3) 기전: Genetic streamlining, Oncogenic shock, Synthetic lethality
• Oncogenic addiction: 암세포는 특정 경로를 통한 신호 전달이 강해지고, 해당 경로를 제외한 나머지 경로를 통한 신호 전달은 불활성화됨 (정상 세포는 여러 경로를 통해 고르게 신호 전달)
① Genetic streamlining: 암세포의 addictive pathway 차단
② Oncogenic shock: addictive oncoprotein 타겟해 death pathway 활성화
③ Synthetic lethality: 두 경로가 하나의 기질에 작용할 때, 두 경로 중 암세포에서 활성화되어 있던 경로 차단
4) 종류
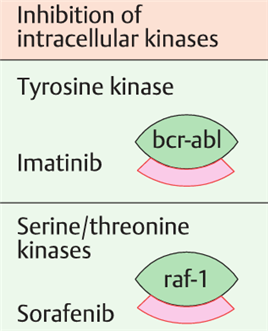
① BCR-ABL kinase 억제제: Imatinib, Dastinib, Nilotinib
• BCR-ABL: 만성골수성백혈병의 필라델피아 염색체(t(9;22)(q34.1;q11.2))에서 발견되는 단백질
• Imatinib의 적응증: CML, Gastrointestinal stromal tumor(c-KIT, PDGFR-α target)
• 내성 발생 기전: BCR-ABL 돌연변이, 암세포의 imatinib 취득률 감소
② ALK 억제제: Alectinib, Crizotinib, Certinib
③ PI3K/Akt/mTOR 억제제: Idelalisib, Sirolimus(Rapamycin), Everolimus
• mTOR1 억제제: Sirolimus(Rapamycin), Everolimus, Temsirolimus
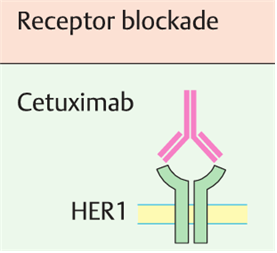
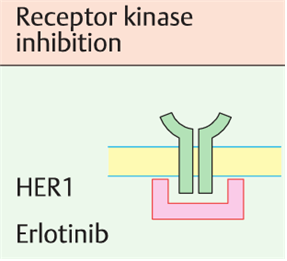
④ EGFR 억제제: Erlotinib, Gefitinib, Cetuximab, Panitumumab
• Cetuximab: Ras 돌연변이 없는 wild type 암종에서 사용(표적과 예후 예측 지표가 다름)
• Cetuximab: 부작용(여드름) 심할수록 생존율 높음
• Gefitinib: EGFR 내에서도 어떤 엑손에 변이가 있는지에 따라 효과 달라짐
⑤ HER2/Neu 억제제: Trastuzumab, Pertuzumab, Lapatinib, Nerpatinib
• HER2(ErbB2 oncogene) 과발현 유방암: 20~30% 환자, 주로 진행형, 항암제/호르몬 치료에 낮은 반응률, 높은 재발률을 보임
• HER2 과발현 정도, 유전자 증폭 정도를 통해 HER2-표적 치료 예측
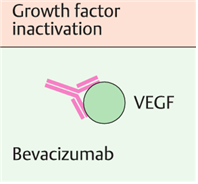
⑥ 혈관 신생 억제제: Bevacizumab(VEGF antibody), Aflibercept, Pazopanib, Sorafenib, Sunitinib
• Aflibercept: 단일클론항체이지만, 여러 표적 물질을 가짐(VEGFA, VEGFB, PIGF)
| | | | |
5) 한계: 표적 치료를 통해 암세포의 특정 경로를 억제되어 암세포가 불활성화되었던 대체 경로를 다시 활성화할 경우 항암제에 대한 내성 획득
6) 내성 기전: ① kinase target 변화 ② Downstream effector 활성화 ③ 기존 addictive pathway bypass
3. 면역항암제
1) 사용: Driver oncogene이 없거나 표적 대상이 없는 경우
2) Cancer-Immunity cycle
① Release of cancer cell antigens(neoantigen)
② Cancer antigen presentation
(+): TNFα, IFNα, IL-1, CD40L/CD40, TLR, ATP, HMGB1
(-): IL-10, IL-4, IL-13
③ Priming and activation
(+): CD28/B7.1, CD137/CD137L, OX40/OX40L, CD27/CD70, HVEM, GITR, IL-2, IL-12
(-): PD-L1/PD-1, CTLA4/B7.1, PD-L1/B7.1, prostaglandins
④ Trafficking of T cells to tumors
(+): CX3CL1, CXCL9, CXCL10, CCL5
⑤ Infiltration of T cells into tumors
(+): LFA1/ICAM1
(-): VEGF
⑥ Recognition of cancer cells by T cells
(+): TCR
⑦ Killing of cancer cells
(+): IFN-γ, T cell granule content
(-): PD-L1/PD-1, IDO, TGF-β, LAG-3, PD-L1/B7.1, BTLA, VISTA, Arginase, MICA/MICB,B7-H4, TIM-3/phospholipids
3) 면역 관문(Immune checkpoint)
Antigen presenting cell | T cell | Cancer cell | |
MHC ↔ T cell receptor (+) B7.2/CD86 ↔ CD28 (+) B7.1/CD80 ↔ CTLA4 (-) | T cell receptor ↔ MHC (+) LAG-3 ↔ MHC (-) B7-1/CD80 ↔ PD-L1(-) PD-1/CD279 ↔ PD-L2(-) | ||
① Priming phase(Lymph node) | ② Effector phase(Tumor site) | ||
4) T세포 조절
(1) Activating receptors: CD28, OX40, GITR, CD137, CD27, HVEM
(2) Inhibitory receptors: CTLA-4, PD-1, TIM-3, BTLA, VISTA, LAG-3
5) 암의 면역 회피: T cell checkpoint dysregulation
① T cell에서 PD-1, CTLA-4↑: PD-1 발현을 증가시켜 T세포 억제, CTLA-4 발현을 증가시켜 T세포의 항원 인식 억제
② 암세포에서 PD-L1↑: T세포 억제
6) 종류
① CTLA-4 억제제(ilu): Ipilimumab
② PD-1 억제제(olu): Nivolumab, Pembrolizumab
③ PD-L1 억제제(alu): Durvalumab, Avelumab, Atezolizumab
7) 효과
① 유전자 변이 여부, 암종에 크게 관계없이 치료 가능
② 기억 T세포 통해 약 중단 이후에도 암세포에 대한 면역 유지
③ 치료 효과 오래 지속
④ 환자 나이와 상관 X
⑤ 효과가 빠르게 나타남
4. 항암제 내성
1) 선천 내성: p53 유전자 소실, mismatch repair gene 결손 등
2) 획득 내성
(1) 다약제내성: MDR(multidrug-resistance)1, MRP(multidrug resistance protein)
• MDR1 유전자: 약물수송 단백질인 P-glyoprotein의 유전정보
• MDR1 발현↑ → 항암제 유출↑ → 항암제의 세포 내 축적↓
• 세포외배출수송체 억제하는 verapamil이나, 다약제병용요법 통해 극복
• MRP: 세포 외 배출 수송체
5. 항암제 부작용
1) 세포독성항암제
(1) 급성 부작용
① Infusion reaction: 알레르기반응, 아나필락시스까지 가능
② Extravasation: 약물 주입 부위 주변 조직 괴사
③ Emesis(Nausea, Vomiting): CINV(chemotherapy induced nausea/vomiting)
• 치료: lorazepam, cannabinoids, olanzapine, gabapentine
(2) 단기 부작용
① Mucositis
② Diarrhea, delayed emesis
③ Hepatic, renal problem
④ Bone marrow suppression
⑤ Hair, skin problem
(3) 장기 부작용
① Cardiac/neuro/gonadal Toxicity
2) 혈관 신생 저해제
(1) 공통 부작용: 고혈압, 단백뇨, 갑상선 저하증, 혈전색전증
(2) ramucirumab, bavacizumab: infusion reaction, amenorrhea, GI perforation
(3) TKI: hand-foot syndrome, skin rash
(4) pazopanib: hepatotoxicity
3) 심독성
(1) doxorubicin: heart failure
(2) trastuzumab: heart failure (Her-2가 심근 형성에 관여)
(3) PD-1/PD-L1 inhibitor: autoimmune myocarditis
4) pulmonary toxicity: bunsulfan, mTOR inhibitor, PD-1/PD-L1 inhibitor
Reference
• Goodman & Gilman’s The pharmacological basis of therapeutics 14th ed, pp.1159-1248
• Katzung&Trevor's pharmacology Examination&Board Review 10th ed, pp.465-490
• Color Atlas of Pharmacology 5th ed, pp. 296-303
• 이우주의 약리학 강의 제8판 789-864쪽