단백질의 구조
이론과 하이라이트 히스토리를 확인 할 수 있어요.
R기, 아미노기, 카복실기로 구성된 단백질의 구조와 일부 단백질의 명칭 혹은 생성, 분해 과정을 묻는 문제가 주로 출제된다. 아미노산의 등전점을 구하거나, pH에 따른 아미노산 구조와 유비퀴틴화 과정이 빈출되므로 이에 대한 명확한 이해가 요구된다. 아직 각 아미노산의 명칭 혹은 R기의 그룹 분류를 묻는 문제는 출제되지 않았다.
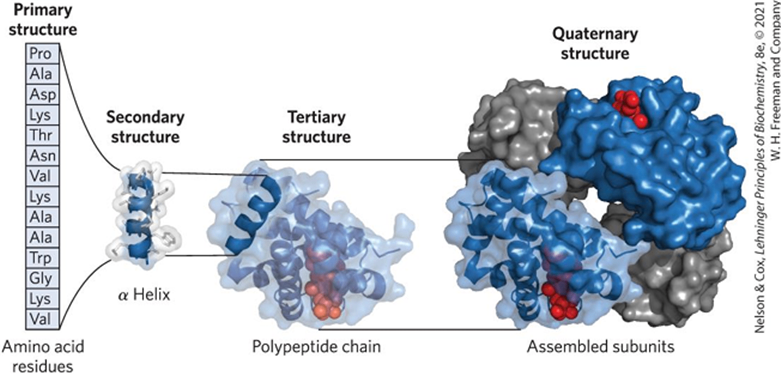
1. 단백질의 구조
1) 1차 구조: 아미노산 서열 + Cysteine 간 이황화결합
(1) N → C 순서로 펩타이드 결합 형성
(2) Cysteine: -SH기를 가져 이황화결합 형성 가능
2) 2차 구조: polypeptide chain 내 아미노산 간 수소결합 (α helix와 β sheet로 구분)
(1) R기 고려하지 않은 구조
(2) 아미노기의 수소와 카복실기의 산소 간 수소결합
(3) α helix breaker(β turn): α helix와 β sheet의 흐름을 연결해주는 요소
• 예시: Proline(ring 구조로 인한 rigidity), Glycine(작은 R기(-H)로 인한 높은 자유도)
3) 3차 구조: polypeptide chain 내 아미노산 간 수소결합, 이온결합, 비극성 소수성 결합을 통해 접힌 3차원 구조 (fibrous와 globular로 구분)
(1) R기 고려
(2) 소수성 상호작용(hydrophobic interaction)이 주요 동력
4) 4차 구조: 독립된 둘 이상의 polypeptide chain이 모여 형성된 구조
• 하나의 polypeptide만으로 구성된 단백질은 4차 구조가 없음 (ex. myoglobin)
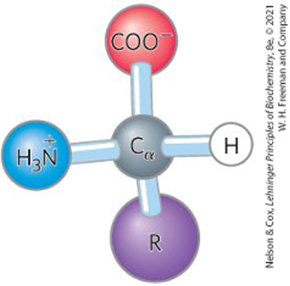
2. 아미노산의 구조
1) 구성: C, H, O, N
2) 구조: Cα(α-carbon, 중심탄소)에 카르복실기(-COO-), 아미노기(-NH3+), 수소 원자, R기가 결합한 형태
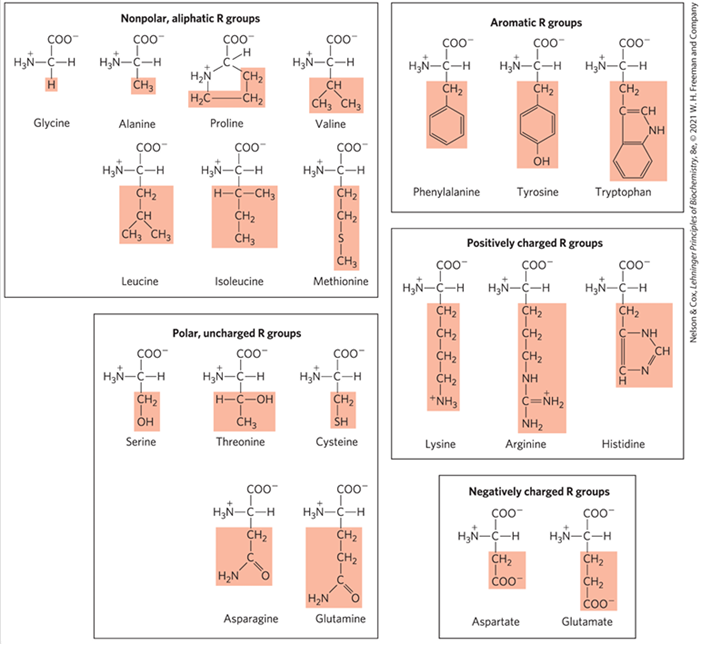
3) 종류: R기에 따라 20가지로 분류 (neutral pH 상황 기준)
(1) Nonpolar, aliphatic R groups: G, A, P, V, L, I, M
(2) Aromatic R groups: Y, W, F
(3) Polar, uncharged R groups: N, Q, T, S, C
(4) Positively charged R groups: K, H, R
(5) Negatively charged R groups: D, E
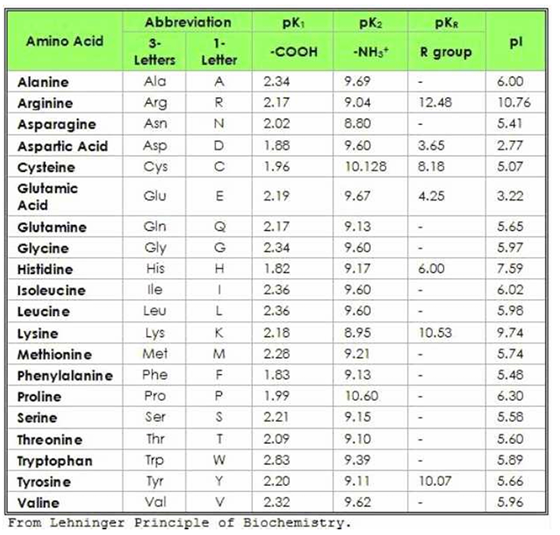
4) 아미노산의 pKa
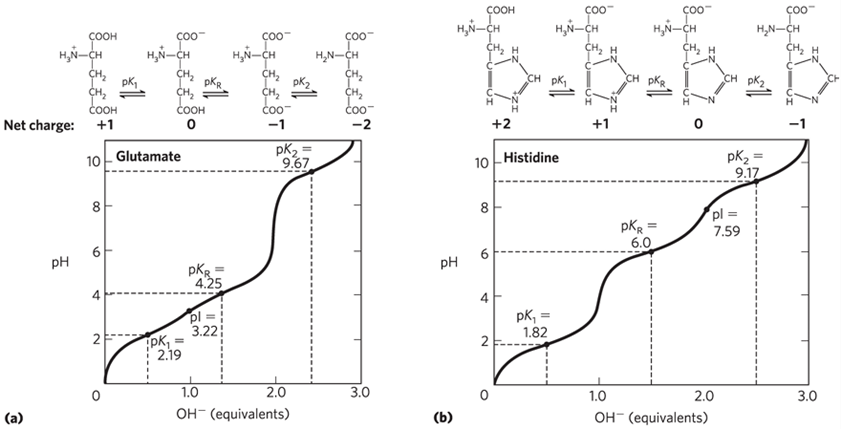
(1) Ka: 산의 해리상수; 해리 상태에서 H+를 쉽게 떼어줄 수 있을수록 Ka가 큼 (2) pKa: –log(Ka); Ka가 클수록 pKa는 작음 (3) pKR: 이온화가 가능한(R기에서 H+가 떼어지는) 7개의 아미노산에 한해 존재 |
5) 적정 곡선(Titration curve)
(1) 산과 염기
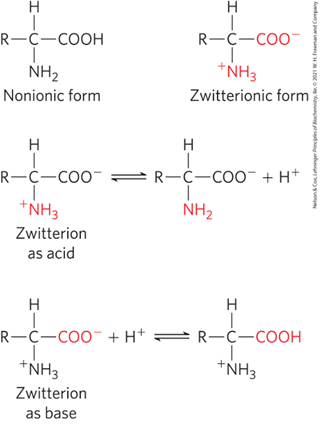
• 산: H+를 떼어주는(deprotonation) 물질 • 염기: H+를 받는(protonation) 물질 |
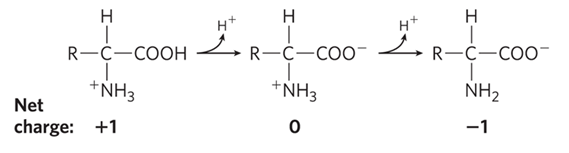
(2) 양쪽성 이온: 모든 아미노산의 작용기(-COOH, -NH2, 일부 –R)는 pH에 따라 약산 또는 약염기 모두로 작용 가능
(3) 핸더슨-하셀바흐식: [HA] → [H+] + [A-]에서 pH = pKa + log([A-]/[HA])
• 특정 pH에서 짝산([HA])와 짝염기([A-])의 비율 계산 가능
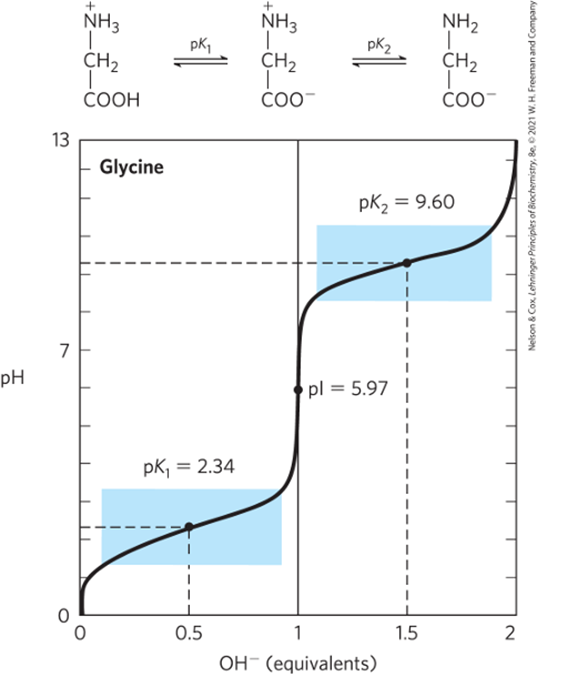
(4) 적정 곡선: pH에 따른 아미노산의 이온화 상태를 보여주는 그래프
• 일반적으로 염기(OH-)를 넣어줌에 따라 –COOH → -NH3+의 순서로 H+가 떨어져 나감 (이온화) (∵pKa: -COOH < -NH3+) • pH = pK1: –COOH 형과 –COO- 형이 같은 비율로 존재 • pH = ( pK1 + pK2) / 2 : 등전점; 양쪽성 이온형(NH3+, COO-)으로 존재 • pH = pK2: -NH3+와 –NH2 형이 같은 비율로 존재 • 이외의 pH: 헨더슨-하셀바흐 공식을 통해 비율 유추 가능 ex. 2.34 < pH < 5.97: –COO- 형(짝염기형) > –COOH 형(짝산형) (∵ pH > pK1) • ionizable R기를 가진 경우 R기의 pKa 값에 따라 적정 곡선의 형태 달라짐. |
(5) 등전점: pH = pI = ( pK1 + pK2) / 2
• 알짜전하량이 0일 때의 pH
• 아미노산의 구조 보고 결정
• Glutamate: pI = ( pK1 + pKR) / 2
• Histidine: pI = ( pKR + pK2) / 2
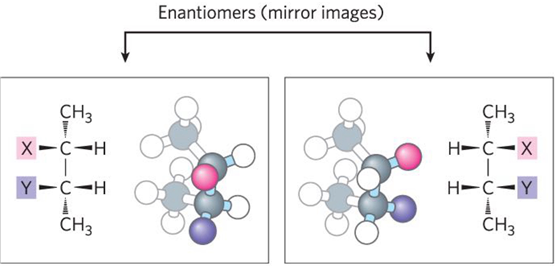
6) 기타 특징: Glycine 제외 모든 아미노산은 거울상 이성질체(enantiomer)를 가짐
3. 단백질의 분해
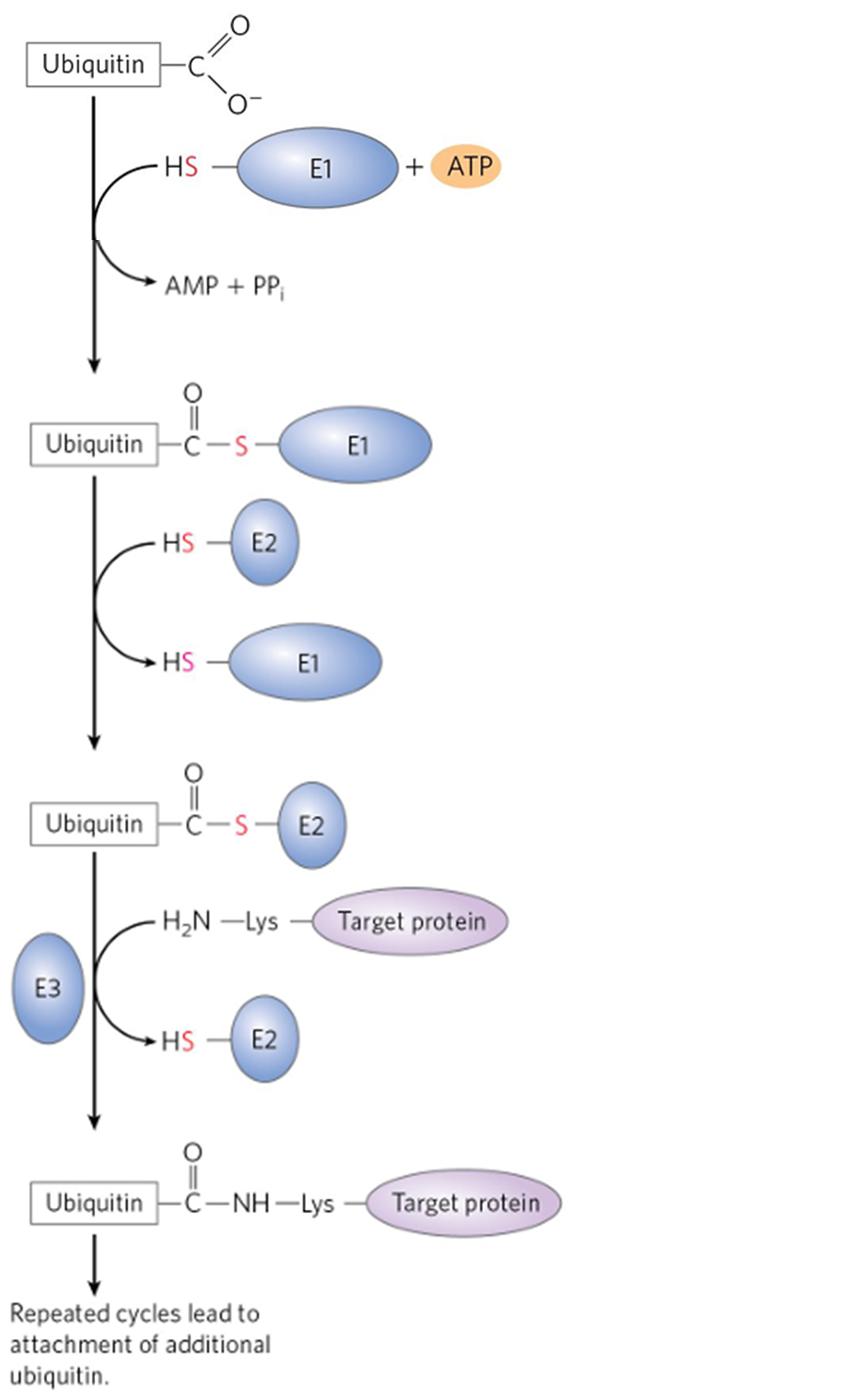
1) Ubiquitination
(1) E1, E2, E3 효소가 표적 단백질에 유비퀴틴 연결해 유비퀴틴 사슬 형성 (2) 프로테아좀이 유비퀴틴 사슬 인식해 표적 단백질 분해 |
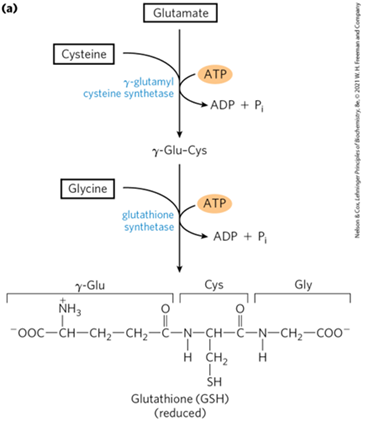
4. 글루타치온
1) 구조: Glutamate–Cysteine-Glycine
2) 역할: Cysteine의 –SH(sulfhydryl)기가 대신 산화되며 항산화제로 작용
3) 형성: Glutamate에 Cysteine과 Glycine이 차례로 결합
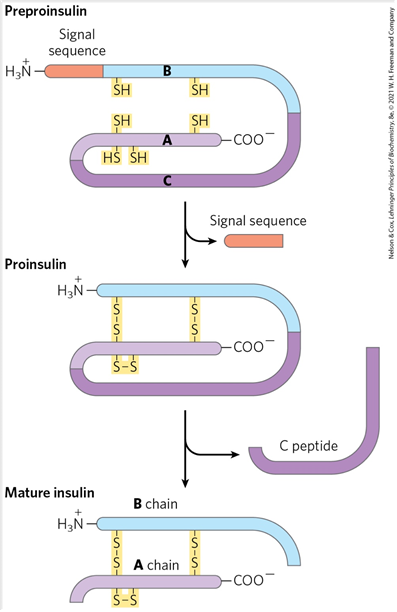
5. 인슐린
1) 구조: A-chain과 B-chain이 두 개의 이황화결합으로 연결된 구조
2) 형성
① ribosome에서 preproinsulin(inactive single-chain precursor) 형성 ② rER 내강에서 신호서열 제거, 이황화결합 통해 proinsulin 형성 ③ 혈당이 오르면 골지체와 분비 과립을 거치며 C(Connecting)-peptide 제거 후 A, B chain 간 이황화결합 통해 mature insulin 형성 |
Reference
• Lehninger Principles of Biochemistry 8th ed, pp. 143. 315-317, 357-597, 2872-2874, 2952-54