단백질의 기능
이론과 하이라이트 히스토리를 확인 할 수 있어요.
헤모글로빈의 생성부터 분해까지 전반적인 내용이 주로 출제된다. 특히 헤모글로빈의 분해, 배출 과정은 번거롭더라도 자세히 읽어보고 황달의 원인별 증상과 연계해보는 것이 좋겠다. 이에 더해 당뇨병과 심근경색의 진단 마커에 관한 내용이 빈출되며, 특히 HbA1c에 대한 자세한 이해가 필요하다.
1. 헤모글로빈
1) 구조: 4개의 글로빈 사슬에 헴 분자가 결합
2) 형성
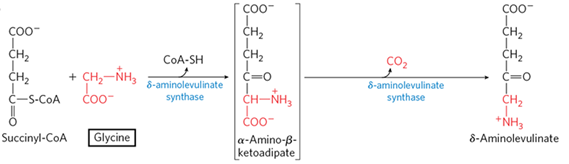
(1) 원료: Succinyl-CoA, Glycine
(2) 과정
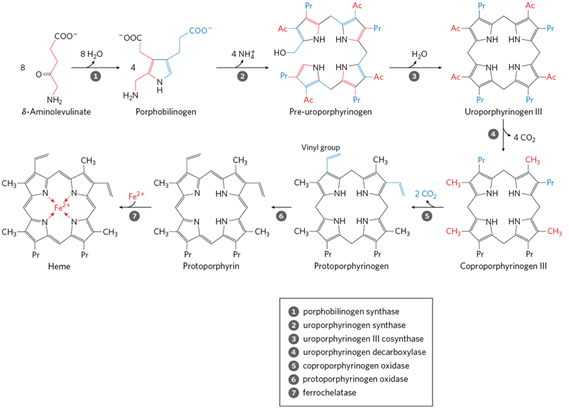
• δ-aminolevulinic acid(ALA) 형성: 미토콘드리아에서 진행, 속도결정단계
• 헴 분자 형성: 세포질에서 진행 후 ⑦만 미토콘드리아에서 진행
(3) 포르피린증(Porphyrias): 헴 합성 과정 문제로 인한 질병의 통칭 → Lab: 헴 결핍, 문제가 생긴 과정 이전의 중간산물 증가
• Tetrapyrrole 형성 이전 과정의 문제: 신경내장성 증상(neurovisceral symptoms)
• Tetrapyrrole 형성 이후 과정의 문제: 광과민성(photosensitivity)
• 치료: 지연피부포르피린증(porphyria cutanea tarda) 제외 사혈요법
3) 산소포화도
(1) 2,3-BPG: 헤모글로빈의 구조를 변형시켜 산소 친화력 저하
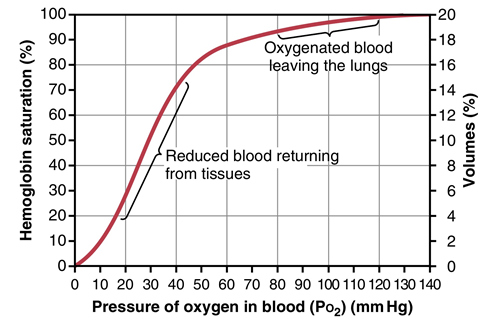
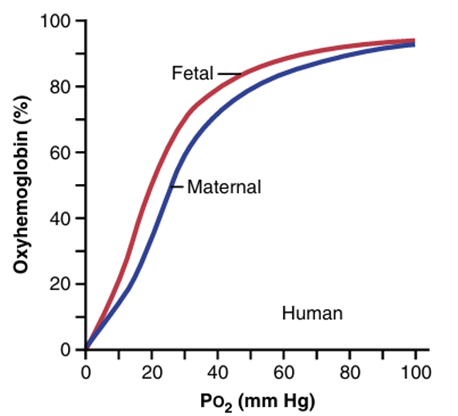
(2) 해리곡선: 산소 분압(PO2)에 따른 헤모글로빈의 산소 포화도(해리도)
• 미오글로빈의 산소 포화도: 산소 분압에만 영향 받음
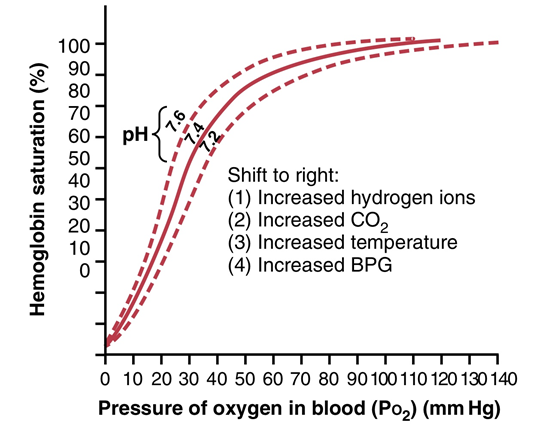
Shift to right | Shift to left | |
Hb의 산소 친화도 | ↓ | ↑ |
예시 | PCO2↑ pH↓ 온도↑ 2,3-BPG↑ | PCO2↓ pH↑ 온도↓ 2,3-BPG↓ 일산화탄소 중독 |
• 산소 친화도: 태아 Hb > 산모 Hb → 산모 혈액에서 태아 혈액으로 산소 이동
3) 변이
(1) 적혈구증가증(erythrocytosis): β-사슬의 82번째 Lysine → Methionine
• Lysine: 양전하를 띄는 R기 → 말단 아민 그룹이 2,3-BPG의 음전하를 띈 인산 그룹과 정전기적 상호작용을 통해 염다리 형성
• Methionine: 전기적 극성을 띄지 않는 R기를 갖기에 2,3-BPG와 염다리 형성 어려움
• 결론: 2,3-BPG에 대한 친화력↓: 헤모글로빈의 산소 친화력↑
(2) β-thalassemia: β-사슬의 점돌연변이
• 증상: 피로감, 관절통, 우상복부 불쾌감, 다뇨증
• Lab: 헤모글로빈↓, 그물적혈구↑, 트렌스페린 포화도↑
• 중동, 아프리카, 동남아시아 지역에서 흔함
(3) 겸상적혈구빈혈증(Sickle cell anemia): β-사슬의 점돌연변이
4) NADPH 결핍
(1) NADPH: 글루타치온 기능 유지 → 산화적 손상으로부터 적혈구 보호
(2) 위험인자: 항말라리아 약물을 통한 적혈구 내 산화 스트레스로 인한 NADPH 수요 증가
(3) 원인: 인산오탄당 경로(PPP)에서의 G6PD(glucose-6-phosphate dehydrogenase) 결핍증
5) 대사
(1) 과정
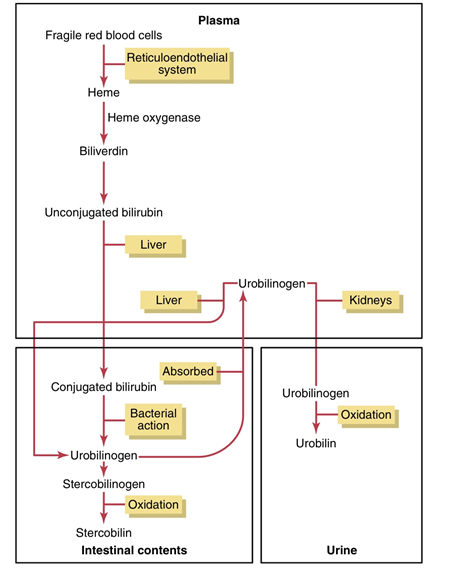
① 세망내피계(Reticuloendothelial system, RES)에서 대식세포가 수명이 다한 적혈구를 헤모글로빈으로 분해
② 헤모글로빈이 heme group(heme + 철)과 글로빈으로 분해, 글로빈은 아미노산으로 분해되어 단백질 합성에 재활용
③ 헴에 있던 철은 트랜스페린에 결합해 골수로 전달되어 적혈구 생산에 재활용
④ 헴은 porphyrin → biliverdin(초록색) → unconjugated bilirubin(UCB, insoluble)로 변환
⑤ UCB는 알부민에 부착해 간으로 이동
⑥ 간에서 Bilirubin glucuronyl transferase (UGT1A1)에 의해 UCB가 conjugated bilirubin(CB, soluble)로 전환 (UCB에 glucuronic acid를 2개 붙여 conjugation)
⑦ CB는 MRP2(multi-drug resistance associated protein 2) 통해 bile duct로 이동
⑧ CB는 bile duct → gallbladder → 소장으로 분비
⑨ 소장 박테리아가 CB를 urobilinogen으로 전환
⑩-1 대부분의 urobilinogen은 대장에서 stercobilin으로 산화, 변으로 배출
⑩-2 일부는 장-간 순환에서 간문맥 통해 간으로 재흡수
⑪ 간으로 재흡수된 urobilinogen 중 일부는 전신순환 통해 신장으로 이동, urobilin이 되어 소변으로 배출
(2) 대사물
• bilirubin: 헴의 주요 분해산물, 황달 유발
• urobilin: 소변 색 결정
• stercobilin: 대변 색 결정
(3) 황달(jaundice): 체내 bilirubin이 축적되어 피부, 손톱, 결막 등이 노란색을 띠는 질병
용혈성 황달 | 폐쇄성 황달 | 간세포성 황달 | |
원인 | 용혈 (sickle cell anemia, malaria 등) → Hb 대량 생성 | 암이나 담석으로 인한 담관 폐쇄 → 장으로의 빌리루빈 이동 억제 | 간 손상 (간염, 간경화) |
conjugated bilirubin | 증가 (∵ Hb 대량 발생) | 혈중 농도 증가 (역류) | 혈중 농도 증가 (역류) |
unconjugated bilirubin | conjugation 한계 도달 →알부민과 결합해 혈액으로 이동 → 혈중 농도 증가 | 축적 (∵ 간의 conjugation 기능 약화) | |
소변 색 | 진해짐 | 진해짐(까매짐) | 진해짐(까매짐) |
대변 색 | 진해짐 | 연해짐, 밝아짐 | 간 손상 진행됨에 따라 점차 연해짐 |
• 신생아 황달: 신생아는 빌리루빈 축적 가능성↑, 발생 시 미성숙한 혈액뇌장벽(BBB)로 인해 치명적, 광선요법(phototherapy) 치료
4. 당화혈색소(HbA1c)
1) 형성: 헤모글로빈이 포도당과 결합(Glycation)해 형성, 적혈구 생존 기간(120일) 동안 결합 상태 유지
2) 활용: 장기간의 혈당 수치 반영 → 당뇨병 치료 효과 확인
3) 특징: 인슐린 치료 시작 후 기존 적혈구가 충분히 소멸되기 전까지 HbA1c 수치 큰 변화 없음 (2~3개월 이상의 시간 필요)
5. 심근경색
1) 진단 마커
(1) 트로포닌(troponin): 최고치 도달 후 3~10일 동안 증가 상태 지속
• 가장 자주 사용
(2) 크레아틴 인산화효소(creatine kinase, CK): 최고치 도달 하루 이틀 후 수치 감소
• 덜 특이적 (골격근 문제에도 수치 상승)
6. 일산화질소(NO)
1) 생성: L-arginine이 NO synthase의 작용으로 L-citruline이 되는 과정에서 발생
2) 역할: 혈관 확장
3) 기전: 평활근 세포의 guanylyl cyclase 활성화 → cGMP↑ → Ca2+↓ → 평활근 수축 억제
7. 알부민
1) 가장 주된 혈장단백질
2) 합성 장소: 간
3) 역할: 혈장 삼투압의 80-90% 담당
4) 결핍
(1) 원인: 간 기능 저하
(2) 증상: 혈장 삼투압 감소 → 혈장 유출 → 부종
5) α-Fetoprotein(AFP): 태아의 알부민 대체 단백질; 임신, 간암 마커
Reference
• Lehninger Principles of Biochemistry 8th ed, pp. 2864-2866
• Guyton and Hall Textbook of Medical Physiology 14th ed, pp.443, 524-528, 875, 1048